浓硫酸与木炭粉在加热条件下反应:C+2H2SO4(浓) CO2↑+2H2O+2SO2↑
CO2↑+2H2O+2SO2↑
Ⅰ、第一小组用下图所示各装置设计一个实验,验证上述反应所产生的三种产物。 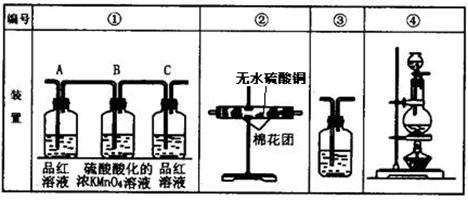
(1)这些装置的连 接顺序(按产物气流从左到右的方向)是(填装置的编号):
接顺序(按产物气流从左到右的方向)是(填装置的编号): ④ →__________→__________→__________。
④ →__________→__________→__________。
(2)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色。A瓶溶液变化体现了SO2 性,B瓶溶液反应是利用SO2 性。
B瓶溶液的作用是 ,
C瓶溶液的作用是 。
(3)实验时装置②中看到现象是 。
(4)装置③中所加的试剂名称是 ,现象是 。
Ⅱ、另一小组为测得CO2和SO2的质量,并算两者物质的量比,设计下列实验:
将生成气体依次通过X溶液→浓硫酸→碱石灰1→碱石灰2,并设法让气体完全被吸收。
(1)下列试剂中可以充当X的是: ( )
| A.BaCl2溶液 | B.Ba(OH)2溶液 |
| C.滴加H2O2的BaCl2溶液 | D.滴加H2O2的Ba(OH)2溶液 |
(2)实验结束后,在X溶液中得到的沉淀通过过滤、洗涤、烘干、称重,称得质量为ag。称得碱石灰1在实验前后 增重质量为bg。用a、b表示CO2和SO2的物质的量比 。
增重质量为bg。用a、b表示CO2和SO2的物质的量比 。
利用废旧锌铁皮制备磁性
胶体粒子及副产物
。制备流程图如下:
已知:
及化合物的性质与
及化合物的性质相似。请回答下列问题:
(1)用
溶液处理废旧锌铁皮的作用有。
| A. | 去除油污 | B. | 溶解镀锌层 | C. | 去除铁锈 | D. | 钝化 |
(2)调节溶液
的
可产生
沉淀,为制得
,后续操作步骤是。
(3)由溶液
制得
胶体粒子的过程中,须持续通入
,原因是。
(4)
胶体粒子能否用减压过滤发实现固液分离?(填"能"或"不能"),理由是。
(5)用重铬酸钾法(一种氧化还原滴定法)可测定产物
中的二价铁含量。若需配制浓度为0.01000
的
标准溶液250
,应准确称取
(保留4位有效数字,已知
=294.0
)。
配制该标准溶液时,下列仪器中不必要用到的有。(用编号表示)。
①电子天平 ②烧杯 ③量筒 ④玻璃棒 ⑤容量瓶 ⑥胶头滴管 ⑦移液管
(6)滴定操作中,如果滴定前装有
标准溶液的滴定管尖嘴部分有气泡,而滴定结束后气泡消失,则测定结果将(填"偏大"、"偏小"或"不变")。
氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗。纯化工业级氧化锌(含有
(Ⅱ),
(Ⅱ),
(Ⅱ)等杂质)的流程如下:
提示:在本实验条件下, (Ⅱ)不能被氧化,高锰酸钾的还原产物是
回答下列问题:
(1)反应②中除掉的杂质离子是,发生反应的离子方程式为。
加高锰酸钾溶液前,若pH较低,对除杂的影响是。
(2)反应③的反应类型为,过滤得到的滤渣中,除了过量的锌外还有。
(3)反应④形成的沉淀要用水洗,检验沉淀是否洗涤干净的方法是。
(4)反应④中产物的成分可能是
.取干操后的滤饼11.2
,煅烧后可得到产品8.1
. 则
等于。
正丁醛是一种化工原料。某实验小组利用如下装置合成正丁醛。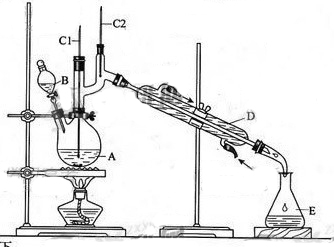
发生的反应如下:
反应物和产物的相关数据列表如下:
| 沸点/℃ |
密度/(
) |
水中溶解性 |
|
| 正丁醇 |
11.72 |
0.8109 |
微溶 |
| 正丁醛 |
75.7 |
0.8017 |
微溶 |
实验步骤如下:
将6.0
放入100
烧杯中,加30
水溶解,再缓慢加入5
浓硫酸,将所得溶液小心转移至
中。在
中加入4.0
正丁醇和几粒沸石,加热。当有蒸汽出现时,开始滴加
中溶液。滴加过程中保持反应温度为90-95℃,在E中收集90℃以下的馏分。将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75-77℃馏分,产量2.0
。
回答下列问题:
(1)实验中,能否将
溶液加到浓硫酸中,说明理由。
(2)加入沸石的作用是。若加热后发现未加沸石,应采取的正确方法是。
(3)上述装置图中,
仪器的名称是,
仪器的名称是。
(4)分液漏斗使用前必须进行的操作是(填正确答案标号)。
a.润湿 b.干燥 c.检漏 d.标定
(5)将正丁醛粗产品置于分液漏斗中分水时,水在层(填"上"或"下")
(6)反应温度应保持在90-95℃,其原因是。
(7)本实验中,正丁醛的产率为%。
醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如下:

可能用到的有关数据如下:
合成反应:
在
中加入20
环己醇和2小片碎瓷片,冷却搅动下慢慢加入1
浓硫酸。
中通入冷却水后,开始缓慢加热
,控制馏出物的温度不超过90℃。
分离提纯:
反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙。最终通过蒸馏得到纯净环己烯10
。
回答下列问题:
(1)装置
的名称是。
(2)加入碎瓷片的作用是;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作时(填正确答案标号)。
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(3)本实验中最容易产生的副产物的结构简式为。
(4)分液漏斗在使用前须清洗干净并;在本实验分离过程中,产物应该从分液漏斗的(填"上口倒出"或"下口放出")。
(5)分离提纯过程中加入无水氯化钙的目的是。
(6)在环己烯粗产物蒸馏过程中,不可能用到的仪器有(填正确答案标号)。
A.圆底烧瓶 B.温度计 C.吸滤瓶 D.球形冷凝管 E.接收器
(7)本实验所得到的环己烯产率是(填正确答案标号)。
A.41% B.50%C.61% D.70%
在现代工业生产中应用广泛。某化学研究性学习小组模拟工业生产流程制备无水
,再用副产品
溶液吸收有毒的
。
Ⅰ.经查阅资料得知:无水
在空气中易潮解,加热易升华。他们设计了制备无水
的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
①检查装置的气密性;②通入干燥的
,赶尽装置中的空气;③用酒精灯在铁屑下方加热至反应完成;④…… ⑤体系冷却后,停止通入
,并用干燥的
赶尽
,将收集器密封。
请回答下列问题:
(1)装置
中反应的化学方程式为。
(2)第③步加热后,生成的烟状
大部分进入收集器,少量沉积在反应管
的右端。要使沉积得
进入收集器,第④步操作是。
(3)操作步骤中,为防止
潮解所采取的措施有(填步骤序号)。
(4)装置
中的冷水作用为;装置
的名称为;装置
中
全部反应完后,因为失去吸收
的作用而失效,写出检验
是否失效的试剂:。
(5)在虚线框内画出尾气吸收装置E并注明试剂
Ⅱ.该组同学用装置
中的副产品
溶液吸收
,得到单质硫;过滤后,再以石墨为电极,在一定条件下电解滤液。
(6)
与
反应的离子方程式为。
(7)电解池中
在阴极放电产生
,阳极的电极反应为。
(8)综合分析实验Ⅱ的两个反应,可知该实验有两个显著优点:①
的原子利用率100%;②。