某化学兴趣小组测定某FeCl3样品(含少量FeCl2杂质)中铁元素的质量分数,实验室按以下步骤进行:
① 称量a g样品,置于烧杯中;
② 加入适量盐酸和适量蒸馏水,使样品溶解,然后准确配制成250mL溶液;
③ 准确量取25.0 0mL步骤②中配得的溶液,置于烧杯中,加入适量的氯水使反应完全;
0mL步骤②中配得的溶液,置于烧杯中,加入适量的氯水使反应完全;
④ 趁热迅速加入过量氨水,充分搅拌,使沉淀完全;
⑤ 过滤,洗涤沉淀;
⑥ 将沉淀转移到坩埚内,加热、搅拌,直到固体全部由红褐色变为红棕色后,在干燥器中冷却至室温后,称量;
⑦ 重复以上操作,至最后两次称得的质量不超过0.1g为止。
请根据上面叙述,回答:
(1)下图所示仪器中,本实验步骤①②③中必须用到的仪器是E、F和 (填字母)。 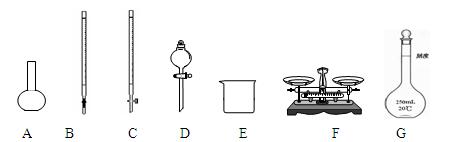
(2)步骤②加入盐酸的目的是 ;加快样品溶解的最简单操作是 。
(3)写出步骤③中发生反应的离子方程式 。
(4)步骤⑤的洗涤是洗去附着在沉淀上的 (写离子符号),洗涤沉淀的操作 。
(5)若坩埚质量是W1,坩埚与加热后固体总质量是W2,则样品中铁元素的质量分数为 。
教材中给出了Na2O2与H2O反应的化学方程式2Na2O2+2H2O=4NaOH+O2↑。为了探究Na2O2与H2O反应的机理,某学习探究小组在教师指导下设计了如图所示装置进行实验。
实验步骤如下:
①按图示组装仪器,并检查装置气密性为良好后装入药品。
②保持K1打开、K2关闭,将注射器中的蒸馏水推入试管中,此时试管中并无气体产生。
③挤压装有酚酞的胶头滴管,使酚酞滴入试管中,试管中溶液显红色。
④挤压装有稀盐酸的胶头滴管,使稀盐酸滴入试管中,红色消失后再滴加2滴。
⑤用双连打气球向A中试管中鼓气,使试管中溶液通过喷头进入B中支管中,发现淀粉-KI溶液变蓝,KMnO4溶液褪色。
⑥迅速打开K2、关闭K1,继续向A中试管中鼓气,待试管中溶液进入C中试管中约三分之一时停止鼓气。然后用热水浴加热C中试管片刻,有气泡冒出,经检验为氧气。
请回答下列问题:
(1)用离子方程式表示淀粉-KI溶液变蓝的原因:_____________________________
________________________________________________________________________。
(2)用离子方程式表示KMnO4溶液褪色的原因: ______________________________
________________________________________________________________________。
(3)A中用冰盐冷浴和C中用热水浴的作用分别是________、______________________。
(4)Na2O2与H2O反应的机理是____________________(用化学方程式表示)。
镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。主要步骤如下:
(1)为了使MgSO4转化为Mg(OH)2,试剂①可以选用________,要使MgSO4完全转化为沉淀,加入试剂的量应为________________。
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是_____________。
(3)试剂②选用________;写出其反应的离子方程式_______。
(4)无水MgCl2在熔融状态下,通电后产生镁和氯气,该反应的化学方程式为________。
实验室中用含少量CO2杂质的CO来还原铁的氧化物FexOy并证明CO能够还原FexOy,且本身被氧化为CO2,实验所提供的各种仪器和药品如下:
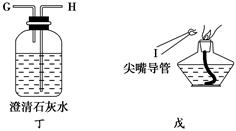
(1)实验时,上述仪器装置的正确连接顺序是(填写各接口的代号)。混合气体―→________,________接(F),(E)接________,________接________,________接________。
(2)在装置乙中发生反应的化学方程式是_______________________。
(3)在装置甲中发生反应的化学方程式是______________。
(4)丙装置中澄清石灰水的作用是_______________。
(5)经定量测定,0.4 g FexOy与CO反应生成的气体通入过量的澄清石灰水中,生成0.75 g白色沉淀,则FexOy中x值是________,y值是________。
(6)实验过程中,能说明CO能够还原FexOy的实验现象是___________。能够说明CO被氧化成CO2的实验现象是____________。
2008年,三鹿等多家乳制品企业为使蛋白质含量检测合格而加入三聚氰胺,使多名儿童患肾结石,实验室可用下列实验装置测定三聚氰胺的分子式。
已知三聚氰胺的相对分子质量为126。取1.26 g三聚氰胺样品,放在纯氧中充分燃烧,生成CO2、H2O、N2,实验测得装置B增重0.54 g,C增重1.32g,排入F中水的体积为672 mL(可按标准状况计算)。
(1)E装置的作用是_____________。
(2)需要加热的装置是____________(填字母代号)。
(3)装置D的作用是_________________________________。
(4)F处读数时应该注意:____________、____________。
(5)三聚氰胺的分子式为_________________。
已知A的产量通常用来衡量一个国家的石油化工发展水平,B、D是饮食中两种常见的有机物,F是一种有香味的物质,F中碳原子数是D的两倍。现以A为主要原料合成F和高分子化合物E,其合成路线如图所示。
(1)A的结构式为____________,B中决定性质的重要官能团的名称为____________。
(2)写出反应的化学方程式并判断反应类型。
①______________________,反应类型:____________。
②_____________________________,反应类型:____________。
(3)实验室怎样鉴别B和D?________________。
(4)在实验室里我们可以用如图所示的装置来制取F,乙中所盛的试剂为____________,该溶液的主要作用是____________________;
该装置图中有一个明显的错误是______________________________。