实验室制取乙烯,常因温度过高而使乙醇和浓H2SO4反应生成少量的二氧化硫,有人设计下列实验以确认上述混合气体中有乙烯和二氧化硫。其装置如右图所示。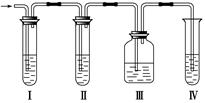
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ装置可盛放的试剂是:
Ⅱ____________;Ⅲ__________;Ⅳ____________(将下列有关试剂的序号填入空格内)。
| A.品红溶液 | B.NaOH溶液 |
| C.浓H2SO4 | D.酸性KMnO4溶液 |
(2)能说明二氧化硫气体存在的现象是____________________________________________________________________
(3)使用装置Ⅱ的目的是_______________________________ ______________________________________
______________________________________
使用装置Ⅲ的目的是______________________________________________________________ _______
_______
(4)确证含有乙烯的现象是_____________________________________________________________________
如图是A、B、C三种固体物质的溶解度曲线图,请回答: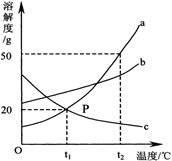
(1)A、B、C三种物质的溶解度受温度影响最大的是 。
(2)P点表示的意义是 。
(3)t2℃时,三种物质的溶解度从大到小的顺序是 。
(4)在t1℃时,将15gC物质加入到50g水中,充分搅拌后,所得溶液中溶质的质量分数为 。
A、B、C、D、E、F六种元素分布在三个不同的短周期,它们的原子序数依次增大,其中B与C为同一周期,D、E、F为同一周期,A与D,C与F分别为同一主族,C元素的原子最外层电子数是次外层电子数的三倍,D是所在周期原子半径最大的元素。又知六种元素所形成的常见单质,在常温常压下,有三种是气体,三种是固体。请回答下列问题:
(1)写出F在周期表中的位置_____ ___。画出D的离子结构示意图___________。
(2)由A、C两元素可以组成X、Y两种化合物,X在一定条件下可以分解成Y,X的电子式为_______________。
(3)C与F形成的常见化合物属于_________晶体。若E的单质是常见的半导体材料,则A与B形成的常见化合物R、C与D形成的常见化合物S、C与E 形成的常见化合物T, R、S、T三者的沸点从高到低排列为____________________(写化学式)
(4)在10L的密闭容器中,通入2molFC2气体和3mol C的气体单质,一定条件下反应后生成FC3气体,当反应达到平衡时,单质C的浓度为0.21 mol·L—1,则平衡时FC2的转化率为________。
(1)今有2H2+O2 =2H2O反应,构成碱性KOH燃料电池,则负极电极反应式为 ,正极电极反应式是 。
(2)若把KOH改为稀H2SO4作电解质,则负极电极反应式为 ;正极电极反应式为 。(1)和(2)的电解质不同,反应进行后,其溶液的pH个有什么变化? 。
(3)若把H2改为CH4,用KOH作电解质,则负极电极反应式为 ;正极电极反应式为 。
依据事实,写出下列反应的热化学方程式。
①在25℃、101kPa下,1g丙醇(C3H7OH)燃烧生成CO2和液态水时放热52.68kJ。则表示丙醇燃烧热的热化学方程式为 ____________
②若适量的N2和O2完全反应,每生成6克NO需要吸收6.8kJ热量。_________ ____
③用NA表示阿伏加德罗常数,在C3H6(气态)完全燃烧生成CO2和液态水的反应中,每有9NA个电子转移时,放出741kJ的热量______________。
④已知火箭燃料液态二甲基肼(CH3—NH—NH—CH3)的完全燃烧30克,产生液态水放出热量898.2kJ,则关于二甲肼燃烧热的热化学方程式__ ___
(1)相对分子质量为72的烷烃的分子式是_____________,
(2)该烷烃在空气中燃烧的化学反应方程式是 ,
(3)它可能的结构简式是 。