下图表示各物质之间的转化关系。已知:A、D、F、H均为单质,X常温下为无色液体,B为淡黄色固体,J溶于酸得到黄色溶液。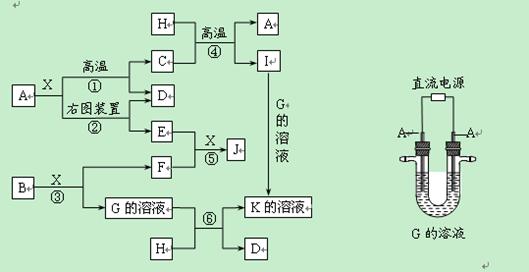
请按要求填空:
(1)写出B的电子式:______________________。
(2)写出生成E的电极反应式:___________________________________________________,反应⑤的现象是______________________________________。
(3)反应①的化学方程式是_____________________________________________________,在实验室中引发反应④的操作是__________________________________________。
(4)反应⑥的离子方程式是_____________________________________________。
某兴趣小组在研究性学习中设计了如下实验来探究Fe和H2SO4反应的过程,装置如下图所示。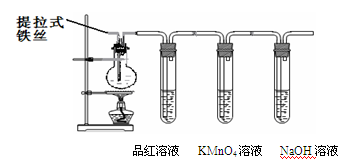
①在烧瓶中加入浓硫酸。
②将提拉式铁丝插入溶液中,观察到有少量气泡,后停止的现象。
③加热烧瓶至有大量气体 产生时停止加热,品红溶液颜色褪去,烧瓶中溶液变为棕黄色。
④一段时间后KMnO4溶液颜色不再变浅,但NaOH 溶液中仍有气体放出,在导管口处可点燃此气体,烧瓶中液体变为浅绿色
根据以上实验回答:
由步骤②的现象可得出的结论是:
在步骤③中,品红溶液褪色的原因是
写出步骤④中,使溶液变为浅绿色的可能的原因是(用离子方程式表示);
(4)KMnO4溶液褪色的化学方程式。
(5)设计实验证明反应后的溶液中只有Fe2+(答操作和现象)
(6)若在反应中铁丝质量减少a克,并收集到bL可燃性气体(标准状况下假设无体积损失),则在反应过程中产生的使品红溶液褪色的气体的质量是(用含a、b数学表达式表示)
(10分)某种胃药片的制酸剂为碳酸钙,其中所含的制酸剂质量的测定如下:
①需配制0.1 mol・L-1的盐酸和0.1mol・L-1的氢氧化钠溶液;
②每次取一粒(药片质量均相同)0.2g的此胃药片,磨碎后加入20.00mL蒸馏水;
③以酚酞为指示剂,用0.1mol・L-1的氢氧化钠溶液滴定,需用去VmL达滴定终点;
④加入25.00mL0.1mol・L-1的盐酸溶液。
(1)写出实验过程中第一次滴定①-④的编号顺序______________。
(2)下图所示的仪器中配制0.1mol・L-1盐酸和0.1mol・L-1氢氧化钠溶液肯定不需要的仪器是(填序号)_________,配制上述溶液还需要的玻璃仪器是(填仪器名称)__________。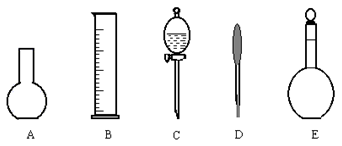
(3)配制上述溶液应选用的容量瓶的规格是(重复滴定一次)__________________。
| A.50mL、50mL | B.100mL、100mL |
| C.100mL、150mL | D.250mL、250mL |
(4)写出有关的化学方程式_____________________。
某学生用0.100 mol·L-1的NaOH标准溶液滴定未知浓度的盐酸,
其操作可分解为如下几步:
| A.移取20.00 mL待测盐酸溶液注入洁净的锥形瓶,并加入2~3滴酚酞; |
| B.用标准溶液润洗滴定管2~3次; |
| C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液; |
| D.取标准KOH溶液注入碱式滴定管至刻度“0”以上2~3 mL; |
E.调节液面至“0”或“0”以下刻度,记下读数;
F.把锥形瓶放在滴定管的下面,用标准NaOH溶液滴定至终点并记下滴定管液面的刻度。
就此实验完成填空:
(1)正确操作步骤的顺序是(用字母序号填写)。
(2)上述A步骤操作之前,若先用待测溶液润洗锥形瓶,则滴定结果(填“偏高”“偏低”或“不变”)。
(3)判断到达滴定终点的实验现象是。
下列实验中,不能达到预期目的的是
①用升华法分离碘和氯化铵的混合物
②用结晶法分离硝酸钾和氯化钠的混合物
③用分液法分离水和硝基苯的混合物
④用蒸馏法分离乙醇(沸点为78.5 ℃)和乙酸乙酯(沸点为77.5 ℃)的混合物
| A.①④ | B.②③ | C.③④ | D.②④ |
某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。请回答下列问题:
(1)装置A中盛放亚硫酸钠的仪器名称是____________________,其中发生反应的化学方程式为_________________________________。
(2)实验过程中,装置B中发生的现象是,说明SO2 具有性;
装置C中发生的现象是,说明 SO2 具有性;
(3)装置D的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象:______________;
(4)尾气可采用溶液吸收。