已知A、J为常见金属单质,常温下B为液体化合物,E是空气的主要成分之一,L是蓝色沉淀,H为红棕色气体;它们之间的转换关系如下图所示: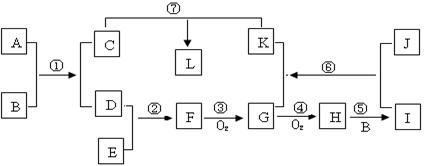
(1)H的化学式是________。
(2)③的化学方程式是__________________________________。
(3)⑥的离子方程式是_______________________________。
(4)F名称是________,检验此气体的方法是___________________________________。
现有A、B、C、D、E五种易溶于水的强电解质,它们由如下离子组成(各种离子不重复)。
| 阳离子 |
H+、NH4+、Mg2+、Ba2+、Al3+ |
| 阴离子 |
OH-、Cl-、HCO3-、NO3-、SO42- |
已知:①0.1 mol/L A溶液的pH <1;②将B溶液分别与其它四种溶液混合,均有白色沉淀生成;
③C溶液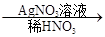 白色沉淀。请回答下列问题:
白色沉淀。请回答下列问题:
(1)写出下列物质的化学式:A______________、B______________。
(2)写出“C溶液 白色沉淀”有关反应的离子方程式____________________________。
白色沉淀”有关反应的离子方程式____________________________。
(3)D、E两种物质中必有一种是_______________,写出将少量该物质的溶液滴加到B溶液中反应的离子方程式___________________________________________________________________。
(4)请你设计实验确定C及另一种未知物各是什么物质。(只许在A~E中选择检验试剂)
| 实验步骤 |
预期现象和结论 |
| 取适量C的溶液于试管中,① 。 |
预期现象和结论1:②; 预期现象和结论2:③; |
有A、B、C、D、E、F六种物质,它们之间相互转化关系如图所示(条件及部分产物未标出)。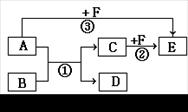
(1)若A、D为气体,都能使澄清的石灰水变浑浊;B、F做焰色反应,透过蓝色钴玻璃观察为紫色, B、C为正盐,F的溶液为紫红色。则C和F在酸性溶液中发生反应②的离子方程式为。
(2)若1 mol A分子中含有3 mol极性共价键, B、C、F都是短周期元素组成的非金属单质;常温下,只有D为固体,其它为气体。则反应③的化学方程式为。
某同学设计了如图所示装置(夹持仪器省略)进行上述(2)中物质B的化学性质探究。
①你认为此装置设计是否合理?若不合理如何改进:。(若合理此问不答)
②Ⅱ中产生的现象是。
③反应几分钟后,检验Ⅲ中可能含有的金属阳离子的实验操作是。
④通过以上探究,气体B的主要化学性质是。
近期曝出的“毒大米”事件,引起了国人的震惊和忧虑,又一次把环境问题摆在了我们面前。“毒大米”是由镉污染引起的,会对人体健康造成严重危害。镉元素在元素周期表中的图示如图所示。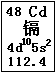
请回答下列问题:
(1)镉元素的原子序数为,在元素周期表中的位置是。
(2)有人说:“‘毒大米’中镉的含量很低,每人每天食用大米量也较少,所以,不会对人体健康造成严重危害。”你对这种说法有何评论?。
(3)你认为“毒大米”中镉的来源是什么?。
(4)镉也是生产电池的重要材料,镉镍二次电池(碱性)的放电和充电反应为:
Cd + 2NiO(OH) + 2H2O Cd(OH)2+ 2Ni(OH)2
Cd(OH)2+ 2Ni(OH)2
电池的负极是。
负极的电极反应式为。
若负极消耗a g反应物,产生N个电子的电量,则阿伏加德罗常数NA=。
T℃时,A、B、C三种气体在反应过程中的浓度变化如图1所示,若保持其它条件不变,温度分别为T1℃和T2℃时,B的浓度变化与时间的关系示意图如图2所示。
请回答下列问题:
(1)该反应的化学反应方程式是:
(2)比较大小:
A和B的转化率AB,原因是
温度的高低T1T2,判断依据是
(3)若其它条件不变,反应进行到(t1+10)min时,A的浓度为
在一固定容积为2 L的密闭容器中加入2 molA和3 molB,保持温度为30℃,在
催化剂存在的条件下进行下列反应:2A(g)+3B(g)  3C(g),2分钟达到平衡,生成1.5 mol
3C(g),2分钟达到平衡,生成1.5 mol
C,此时,平衡混合气中C的体积分数为ω1;若将温度升高到70℃后,其他条件均不变,当
反应重新达到平衡时,C的物质的量为2.1 mol,体积分数为ω2,请回答下列问题,
(1)该反应在30℃时平衡常数K1=,焓变△H0(填“>”、“<”或“=”)。
(2)该反应在30℃时平衡混合气中C的体积分数为ω1=;从反应开始到达到化学平衡状态时v(A)=____________mol/(L·min)
(3)该反应在70℃时平衡常数为K2,则 K1K2(填“>”、“=”或“<”)
(4)70℃时,若保持温度不变,在2 L的密闭容器中加入4 molA和6 molB,当反应重新达到平衡时,C的体积分数为ω3,则ω3ω2 (填“>”、“<”或“="”" )。
(5)可以判断2A(g)+3B(g)  3C(g) 反应已经达到平衡的是( )
3C(g) 反应已经达到平衡的是( )
A.2v(B)=3v(A)
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变
D.混合气体的平均相对分子质量不再改变
E.n(A)∶n(B)∶n(C)=2∶3∶3