甲醇是一种非常好的燃料。熔点-97.8°C,沸点64.5°C。一定条件下,CO与H2反应可制得甲醇:CO+2H2 CH3OH
CH3OH
图1表示该反应进行过程中的能量变化;
图2表示100°C,在体积为2L的恒容容器中加入4molH2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化情况。
(1)已知CO的燃烧热为283kJ/mol,H2的燃烧热为285.8kJ/mol,写出表示CH3OH燃烧热的热化学方程式 。
(2)根据上图2计算:该温度下,反应CO(g)+2H(g) CH3OH(g)的平衡常数为 10min后,容器内的压强变为原来的 倍;改变下列条件,能提高CO转化率的是 。
CH3OH(g)的平衡常数为 10min后,容器内的压强变为原来的 倍;改变下列条件,能提高CO转化率的是 。
A.降低温度 B.加催化剂
C.充入氩气,使体系压强增大 D.再充入1molCO和2molH2
E.恒温恒容改为恒温恒压
(3)已知:CH3OH可以在一定条件下转化为HCOOH,HCOOH和CH3COOH性质相似。25°C,0.1mol/L的HCOOH溶液的pH>1。室温下,向0.1mol/L的HCOOH中加NaOH。
①当溶液中离子浓度关系满足c(HCOO-)<c(Na+)时,则反应的情况可能为 ;
A.NaOH不足,HCOOH剩余 B.HCOOH与NaOH恰好完全反应
C.NaOH过量
②若加入过量的NaOH,在加入NaOH的过程中,H2O的电离程度如何变? 。
判断含氧酸强弱的一条经验规律是:含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性越强。如下表所示
(1)亚磷酸(H3PO3)和亚砷酸(H3AsO3)分子式相似,但它们的酸性差别很大,H3PO3是中强酸,H3AsO3既有弱酸性又有弱碱性。由此可推出它们的结构式分别为 、
、 。
。
简述二者酸性强弱原因_____________________。
(2)亚磷酸和亚砷酸与过量的氢氧化钠溶液反应的化学方程式分别为:
①___________________; ②_______________________。
下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
| A |
|||||||||||||||||
| b |
c |
d |
e |
f |
|||||||||||||
| g |
h |
i |
j |
k |
l |
m |
|||||||||||
| n |
o |
||||||||||||||||
试回答下列问题:
(1)请写出元素O的基态原子电子排布式 。
(2)第三周期8种元素按单质熔点高低的顺序如图,其中序号“8”代表(填元素符号);其中电负性最大的是 (填右图中的序号)第三周期第一电离能介于铝和磷之间的第三周期元素有 种。
(3)由j原子跟c原子以1 : 1相互交替结合而形成的晶体,晶型与晶体j相同。两者相比熔点更高的是(填化学式),试从结构角度加以解释:________________________。
(4)k l 2的电子式是 ,它在常温下呈液态,形成晶体时,属于晶体。
已知N、P同属于元素周期表的第VA族元素,N在第2周期,P在第3周期。NH3分子呈三角锥形,氮原子位于锥顶,三个氢原子位于锥底,N—H键间的夹角是107°。
(1)PH3分子与NH3分子的构型关系是________(填“相同”或“相似”或“不相似”),P—H______极性(填“有”或“无”),PH3分子________极性(填“有”或“无”)。
(2)NH3与PH3相比,热稳定性________更强(填化学式)。
(3)NH3、PH3在常温、常压下都是气体,但NH3比PH3易液化,其主要原因是________.
| A.键的极性N—H比P—H强 |
| B.分子的极性NH3比PH3强 |
| C.相对分子质量PH3比NH3大 |
| D.NH3分子之间存在特殊的分子间作用力 |
(4)笑气(N2O)是一种麻醉剂,有关理论认为N2O与CO2分子具有相似的结构(包括电子式)。已知N2O分子中氮原子只与氧原子相连,N2O的电子式为____,其空间构型是____,由此可知它是____(填“极性”或“非极性”)分子。
某芳香族化合物与苯酚无论以何种比例混合,只要总物质的量一定,完全燃烧时所消耗的氧气和生成水的质量始终一定。试回答:
(1)这类物质的相对分子质量与苯酚的相对分子质量之差为______的倍数(填数字)。
(2)现有这类物质中相对分子质量最小的物质A,已知A溶液能与NaHCO3反应放出气体。现取2.320g苯酚与A的混合物与50.00mLl.000mol/L的Na0H溶液充分反应后,加水至l00mL。取出其中的10.00mL用0.100 /L的
/L的 溶液滴定过量的NaOH,消耗20.00mL时至滴定终点。
溶液滴定过量的NaOH,消耗20.00mL时至滴定终点。
①该过程必须用的定量仪器除了电子天平外还有______、______。
②求该混合物中苯酚的质量分数(结果保留三位有效数字)。
有机物A是一种广谱高效食品防腐剂,图甲是A分子的球棍模型。回答问题: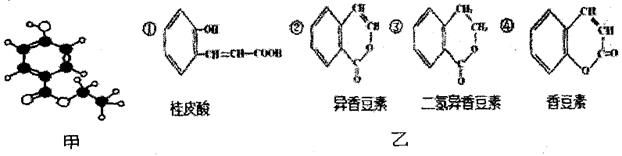
(1)写出A中含有官能团的名称_____________________、_____________________。
(2)A的一种同分异构体B在一定条件下可转化为二氢异香豆素,B的结构简式为____________________
(3)图乙中是一些中草药中所含的有机物:其中互为同分异构体的是(填写序号):____________;不能与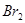 水反应的是(填写序号):______________;
水反应的是(填写序号):______________;
(4)A的另一种同分异构体C遇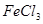 溶液显紫色;l
溶液显紫色;l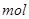 C可与l
C可与l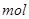 NaOH反应生成有机物D;D被
NaOH反应生成有机物D;D被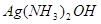 溶液氧化后经酸化得有机物E,E经醇化、消去两步反应可得香豆素,写出符合上述要求的一种C的结构简式:___________________________;
溶液氧化后经酸化得有机物E,E经醇化、消去两步反应可得香豆素,写出符合上述要求的一种C的结构简式:___________________________;
(5)写出A与烧碱溶液反应的化学方程式:______________________________________。