相对分子质量为58的烃或烃的含氧衍生物有多种。请写出符合下列条件的结构简式。
(1)分子结构中含有三个—CH3的是 ;
(2)分子结构中有一个—CH3,且能发生银镜反应的是 ;
(3)分子结构中无—CH3,也无—OH,但能发生银镜反应的是 ;
(4)能和金属钠反应且不能使溴的四氯化碳溶液褪色的化合物 。
因“召回门”而闹的沸沸扬扬的丰田Prius属第三代混合动力车,可以用电动机、内燃机或二者结合推动车轮。汽车上坡或加速时,电动机提供推动力,降低了汽油的消耗;在刹车和下坡时电动机处于充电状态。
(1)混合动力车的内燃机以汽油为燃料,汽油(以辛烷C8H18计)和氧气充分反应,每生成1 mol水蒸气放热569.1 kJ。则该反应的热化学方程式为_________________________________。
(2)混合动力车的电动机目前一般使用的是镍氢电池,镍氢电池采用镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解液。镍氢电池充放电原理示意如图,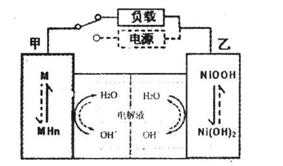
其总反应式是:
根据所给信息判断,混合动力车下 坡或刹车时,甲电极的电极反应式为_______;混合动力车上坡或加速时,乙电极的电极反应式为_________________。
坡或刹车时,甲电极的电极反应式为_______;混合动力车上坡或加速时,乙电极的电极反应式为_________________。
(3)汽车尾气中的一氧化碳是大气污染物,可通过如下反应降低其浓度: CO(g)+1/2O2(g) CO2(g)。
CO2(g)。
①某温度下,在两个容器中进行上述反应,容器中各物质的起始浓度及正逆反应速率关系如下表所示。请填写表中的空格。
| 容器编号 |
c(CO)/mo1·L-1 |
c (O2)/mol·L-1 |
c (CO2)/mol·L-1 |
v(正)和v (逆)比较 |
| I |
2.0×10-4 |
4.0×10-4 |
4.0×10-2 |
v(正)=v(逆) |
| Ⅱ |
3.0×10-4 |
4.0×10-4 |
8.0×10-2 |
②相同温度下,某汽车尾气中CO、CO2的浓度分别为1.0×10-5mol·L-l和1.0×10-4mol·L-l。若在汽车的排气管上增加一个补燃器,不断补充O2并使其浓度保持为1.0×10-4mol·L-1,则最终尾气中CO的浓度为_________mol·L-1。
氯化亚铜是一种重要的化工产品,常用作有机合成催化剂,还可用于颜料, 防腐等工业。该物质露置于空气中易被氧化为绿色的高价铜盐,在热水中易水解生成氧化铜水合物而呈红色。已知pH为5时,+2价铜已开始以碱式盐的形式沉淀。某兴趣小组去一家回收含铜电缆废料的工厂做社会调查,技术人员向他们展示了处理废料的综合利用方案: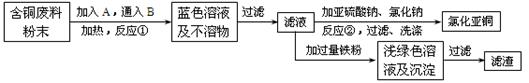
⑴ 加入的A是,通入的B是。
⑵ 反应②的离子方程式是。为提高Cu2Cl2的产率,常在反应②的溶液中加入适量稀碱溶液,控制pH为3.5。这样做的目的是。
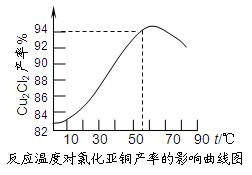
⑶ 保持各反应物的最佳配比,改变温度,测得Cu2Cl2产率的变化如下图所示。则溶液温度控制在时,Cu2Cl2的产率已达到94%,当温度高于65℃时,Cu2Cl2产率会下降,其原因可能是。
高血脂症是现代人的健康杀手之一,科学家最新研制的一种可用于治疗高血脂的新药H可按如下路线合成。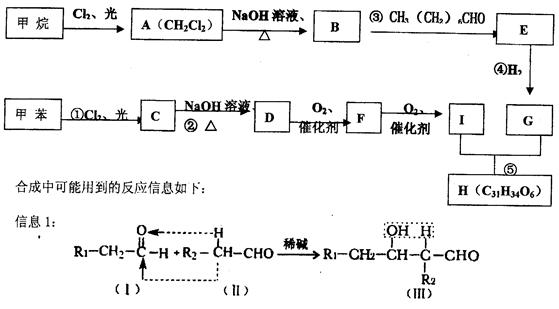
信息2:两个羟基同时连在同一个碳原子上的结构是不稳定的,会发生脱水反应: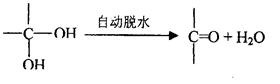
根据以上图示和信息,回答下列问题:
(1)反应①—⑤中属于取代反应有(填写反应的编号),B中官能团的名称为
。
(2)完全燃烧时,1mol D与1mol下列的耗氧量相同(填写字母的代号)。
a. C6H6 b. C7H8O3 c. C6H10O2 d. C7H8O
(3)G的分子式为C10H22O3,写出E、F结构简式:
EF
(4)写出与I互为同分异构体,且既含有苯环又能发生银镜反应的物质的结构简式
、、、
(5)写出F与新制氢氧化铜悬浊液反应的化学方程式:
(6)写出H与NaOH溶液共热的化学方程式
A、Z、R、D、E、F、G是七种原子序数依次增大且不大于20的元素,其中有两种非金属元素位于同一土族。己知A、Z、D均能与R形成原子(或离子)个数不同的儿种常见化合物。请回答下列有关问题。
(1)若X、Y是D、F形成的最高价氧化物对应的水化物,浓度均为0.1mol/L的X、Y溶液的pH之和为14,则X、Y的晶体熔点相对高低为(写化学式),导致这种差异存在的原因是在相同温度下,相等物质的量浓度的X、Y各自的溶液中,由水电离出的c(H+)的相对大小关系为。
(2)A与Z、E均可形成正四面体构型的气态分子Q、P,又知P的燃烧热为1430kJ/mol.则其燃烧的热化学方程式。
(3)R与D、F间;R与F、G间均可形成多种化合物,其中有两种是目前广泛使用的具有消毒杀菌能力的化合物。则相同物质的量浓度的这两种物质的溶液,消毒杀菌能力较强的物质的化学式为,另一种物质的溶液中,各离子浓度由大到小的顺序为。
(4)上述七种元素间能形成多种常见二元化合物,其中Z与G形成的一种化合物存在两类化学键的物质溶于HC1溶液的化学反应方程式为,ZR2的电子式是,该分子的空间构型为化合物ZRF2的结构式为____
(5)R能形成多种单质,如R2、R3,研究表明,新近制得的一种组成为R4的分子中,每个R原子均与另外两个R原子各形成一个键,则1molR4中共用电子对数为____NA,列有关R4的说法中正确的是
①R4与R3、R2互为同位素
②R4不能与A、Z、D的单质反应
③R4中各原予最外层均为8电子结构
④R4是1种新型化合物
在氧化还原反应中,氧化过程和还原过程是同时发生的。
Cu2O—2e-+2H+=2Cu2++H2O是一个氧化过程的反应式,下列五种物质FeSO4、Fe2(SO4)2、CuSO4、Na2CO3、KI中的一种能使上述氧化过程顺利发生。
(1)写出并配平该反应的离子方程式:;
反应中氧化剂和还原剂的物质的量之比是。
(2)向(1)中反应后的溶液里,加入酸性高锰酸钾溶液,反应的离子方程式为
;CH2+、MnO4、Fe3+的氧化性由强到弱的顺序是(用离子符号表示)。