可逆反应:X+Y W+Z,反应速率(V)随时间(t)变化的情况如图所示。
W+Z,反应速率(V)随时间(t)变化的情况如图所示。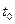 表示在其他条件不变的情况下,改变体系的一个条件(温度、浓度、压强)所引起的变化。则下列分析正确的是
表示在其他条件不变的情况下,改变体系的一个条件(温度、浓度、压强)所引起的变化。则下列分析正确的是
A.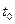 时条件改变引起的变化是平衡向正反应方向移动 时条件改变引起的变化是平衡向正反应方向移动 |
B.若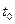 改变 改变 的条件是压强,则W、Z均为气体,X、Y中只有一种为气体 的条件是压强,则W、Z均为气体,X、Y中只有一种为气体 |
C.若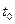 改变的条件是温 改变的条件是温 度,则该反应的正反应是吸热反应 度,则该反应的正反应是吸热反应 |
D.若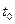 改变的条件是浓度,改变的方法是减小X、Y的浓度 改变的条件是浓度,改变的方法是减小X、Y的浓度 |
下列判断错误的是:( )
| A.将等物质的量浓度、等体积的Ba(OH)2溶液和NaHS04溶液混合,生成白色沉淀:Ba2++SO42‾+H++OH‾ =BaSO4↓+H2O |
| B.常温下,等物质的量浓度的三种溶液①(NH4)2CO3;②NH4Cl;③(NH4)2Fe(SO4)2中c(NH4+):①<②<③ |
| C.加入苯酚显紫色的溶液中:K+、NH4+、Cl-、I- 四种离子不能大量共存 |
D.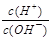 =1×10-12的溶液: K+、AlO2-、CO32-、Na+四种离子可以大量共存 =1×10-12的溶液: K+、AlO2-、CO32-、Na+四种离子可以大量共存 |
会生活密切相关,下列说法正确的是:( )
| A.PM2.5是指空气中直径≤ 2.5 μm的颗粒物,直径为2.5 μm的颗粒物分散在空气中形成胶体(1μm =10 -6 m) |
| B.甲壳素、棉花、铜氨纤维、涤纶、光导纤维都是有机高分子材料 |
| C.有一种新发现的固态碳,称为“纳米泡沫”,外形似海绵,密度小,有磁性,这种碳与金刚石的关系是同素异形体 |
| D.亚硝酸钠是有毒物质,不能添加到食物中 |
向甲乙两个容积均为1L的恒容容器中,分别充入2molA、2molB和1molA、1molB,相同条件下,发生下列反应A(g)+B(g) xC(g) △H<0,测得两容器中c(A)随时间t的变化如图所示,下列说法正确的是
xC(g) △H<0,测得两容器中c(A)随时间t的变化如图所示,下列说法正确的是
A.x等于2
B.向平衡后的乙容器中充入氦气可使c(A) 增大
C.将乙容器单独升温,可使乙容器中各物质的体积分数与甲容器内的相同
D.若向甲容器中再充入2 molA、2 molB,则平衡时甲容器中0.78 mol·L-1<c(A)<1.56 mol·L-1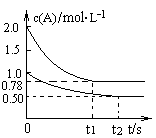
下列实验装置或操作能达到实验目的的是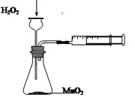


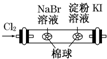
ABC D
| A.定量测定反应速率 | B.验证Na和水反应的热效应 |
| C.酸碱中和滴定 | D.证明氧化性Cl2>Br2>I2 |
下列方程式中正确的是
| A.FeCl2溶液滴加碘水:2Fe2++I2=2Fe3++2I— |
| B.双氧水中滴加2滴FeCl3溶液:2Fe3++H2O2=2Fe2++O2↑+2H+ |
| C.双氧水加入稀硫酸和KI溶液: H2O2+2H++2I—= I2+ O2↑+2 H2O |
| D.在Mg(OH)2悬浊液中滴加氯化铵溶液:Mg(OH)2+2NH4Cl=2NH3·H2O+MgCl2 |