现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,其中物质E是气体丙的水溶液,物质H是红褐色沉淀。它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。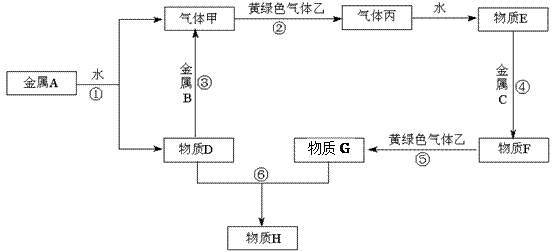
请根据以上信息回答下列问题:
⑴写出A、C、丙的化学式:
A 、 C 、 丙
⑵写出反应③的化学方程式: ,
反应⑤的离子方程式: 。
(9分) 某化学反应2A(g)  B(g)+D(g)在密闭容器中分别在下列四种不同条件下进行,B、D起始浓度均为0,反应物A的浓度(mol•L-1)随反应时间(min)的变化情况如下表:
B(g)+D(g)在密闭容器中分别在下列四种不同条件下进行,B、D起始浓度均为0,反应物A的浓度(mol•L-1)随反应时间(min)的变化情况如下表:
| 时间 实验序号 |
1 |
10 |
20 |
30 |
40 |
50 |
60 |
|
| 1 |
800 ℃ |
1.0 |
0.80 |
0.67 |
0.57 |
0.50 |
0.50 |
0.50 |
| 2 |
800 ℃ |
c2 |
0.60 |
0.50 |
0.50 |
0.50 |
0.50 |
0.50 |
| 3 |
800 ℃ |
c3 |
0.92 |
0.75 |
0.63 |
0.60 |
0.60 |
0.60 |
| 4 |
820 ℃ |
1.0 |
0.40 |
0.25 |
0.20 |
0.20 |
0.20 |
0.20 |
根据上述数据,完成下列填空:
(1)实验1中,在10~20 min时间内,以A的速率表示的平均反应速率为
mol•L-1•min-1。
(2)实验2中,A的初始浓度c2=mol•L-1,反应经20min就达到平衡,可推测实验2中还隐含的条件是。
(3)设实验3的化学反应速率为v3,实验1的化学反应速率为v1,则v3v1(填“>”“=”或“<”),且c3 =mol•L-1
(4)比较实验4和实验1,可推测该反应的正反应是反应(填“吸热”或“放热”),理由是。
(12分)化学实验是研究物质性质的基础。
(1)下列有关实验操作或测量数据不合理的是______(填序号)。
A.用铁坩埚加热CuSO4·5H2O晶体测定结晶水质量分数
B.用干燥的pH试纸测定浓硫酸的pH
C.用规格为20 mL的量筒,量取16.8 mL的Na2CO3溶液
D.用已知浓度盐酸滴定未知浓度氨水,用酚酞做指示剂。
(2) 某废水样品中含有一定量的Na+、CO 、SO
、SO ,某研究小组欲测定其中SO
,某研究小组欲测定其中SO 的浓度。
的浓度。
实验方案:
ⅰ.用烧杯盛取废水适量,加少量活性炭,除去废水中的杂质;过滤,取滤液;
ⅱ.精确量取20.00 mL过滤后废水试样,选择使用紫色的0.1 mol·L-1 KMnO4(H2SO4酸化)溶液进行滴定;
ⅲ.记录数据,消耗KMnO4(H2SO4酸化)溶液体积Vml,计算。
①下列滴定方式中,最合理的是(夹持部分略去)________(填字母序号)。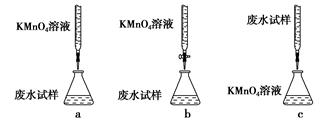
②达到滴定终点时现象是:。SO 的浓度的表达式为:。
的浓度的表达式为:。
(3) 已知反应: BeCl2+Na2BeO2+2H2O =" 2" NaCl+2Be(OH)2 ↓能进行完全, 据此判断下列叙述正确的是:
A、BeCl2溶液的 pH<7, 将其蒸干灼烧后得到的残留物为 Be(OH)2
B、Na2BeO2溶液的 pH>7, 将其蒸干灼烧后得到的残留物为 BeO
C、Be(OH)2既能溶解于盐酸, 又能溶解于 NaOH 溶液
D、Na2BeO2溶液中守恒关系有:C(Na+)+ C(H+)= 2c(BeO22-)+C(OH-)+C(H2BeO2)
E 、Li 、 Be 、 B 三种元素的第一电离能异常小的 B 元素。
(6分)已知某元素的原子序数排在氪元素的原子序数之前,当此元素的原子失去3个电子后,它的角量子数为2的原子轨道内,电子恰好为半充满,则该元素的名称 ,位于第 周期,第 族。
(18分)用“>”或“<”回答下列问题:
(1)酸性:H2CO3______H2SiO3,H2SiO3______H3PO4。
(2)碱性:Ca(OH)2________Mg(OH)2,Mg(OH)2______Al(OH)3。
(3)气态氢化物的稳定性:H2O________H2S,H2S______HCl。
由以上答案可以归纳出:
①元素的非金属性越强,其最高价氧化物的水化物的酸性越________。
②元素的金属性越强,其最高价氧化物的水化物的碱性越________。
③元素的非金属性越强,其对应的气态氢化物的稳定性越________。
(8分)在Fe3O4 +4CO 3Fe+4CO2中, ______是氧化剂,是还原剂,元素被氧化,元素被还原。
3Fe+4CO2中, ______是氧化剂,是还原剂,元素被氧化,元素被还原。