有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的A为无色粘稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
| 实验步骤 |
解释或实验结论 |
| (1)称取A 9.0g,升温使其汽化,测其密度是相同条件下H2的45倍。 |
试通过计算填空: (1)A的相对分子质量为: 。 |
(2)将此9.0gA在足量纯O2充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现分别增重5.4g和 13.2g。 13.2g。 |
(2)A的分子式为: 。 |
| (3)另取A 9.0g,跟足量的NaHCO3粉末反应,生成2.24LCO2(标准状况),若与足量金属钠反应则生成2.24LH2(标准状况)。 |
(3)用结构简式表示A中含有的官能 团: 。 |
(4)A的核磁共振氢谱如下图: |
(4)A中含有 种氢原子。 |
| (5)综上所述,A的结构简式为: 。 |
已知某温度下,KW=1×10-13。A为酸溶液,其pH=a;B为碱溶液,其pH=b。
(1)若A为强酸,B为强碱,且a+b=13,两者等体积混合后,溶液的pH=________;若此时溶液中碱的阳离子浓度大于酸根阴离子浓度,其原因可能是(用文字表述)_____________________。
(2)若A为强酸,B为强碱,二者按体积比为1:10混合后溶液显中性,则a+b=____。
(3)若A的化学式为HR,B的化学式为MOH,且a+b=13,两者等体积混合后溶液显碱性。则混合溶液中必定有一种离子能发生水解,该水解反应的离子方程式为_________________________________。
(4)在(3)的混合溶液中,微粒浓度大小关系一定正确的是___________(填序号)。
①c(MOH)>c(M+)>C(R-)>c(H+)>c(OH-)
②c(HR)>c(M+)>c(R-)>c(OH-)>c(H+)
③c(R-)>c(M+)>c(H+)>c(OH-)
④c(M+)>c(R-)>c(OH-)>c(H+)
⑤c(M+)+ c(H+)=c(R-)+c(OH-)
⑥c(MOH)=c(H+)-c(OH-)
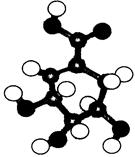
请回答下列问题:
(1)M的结构简式是 。
(2)下列关于M的说法,正确的是
| A.遇FeCl3溶液呈紫色 |
| B.遇紫色石蕊溶液变红色 |
| C.遇溴水发生取代反应 |
| D.能缩聚为高分子化合物 |
(3)M在一定条件下发生消去反应,生成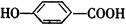 ,该反应的化学方程式是
,该反应的化学方程式是
。
(4)M与有机物A在一定条件下可生成一种相对分子质量为202的酯类物质。A可能的结构简式是 。
(5)研究发现,有一种物质B的分子组成和M完全一样,但分子中无环状结构;B在一定条件下水解能够产生甲醇;B的核磁共振氢谱如下图(两个峰面积比为2:3)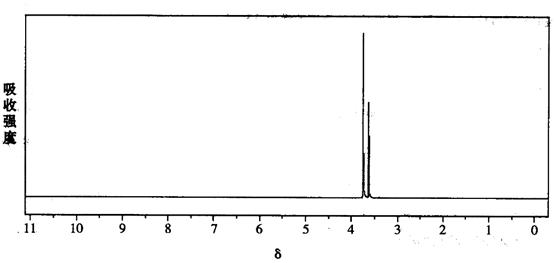
物质B的结构简式是: 。
| 物质 |
NaCl |
MgCl2 |
AlCl3 |
SiCl4 |
| 沸点/℃ |
1465 |
1412 |
181(升华) |
57.6 |
①从表中的数据,结合学过的化学知识,你能得到的规律是。
②以上四种物质中,属于共价化合物的是。
③若你得到的规律具有普遍性,则以下两种物质的沸点高低是:LiClBCl3(填“>”、“==”、“<”)。
(2)在密闭容器中,将1.0mol CO与1.0mol H2O混合加热到800℃,发生下列反应:
CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
一段时间后该反应达到平衡,测得CO的物质的量为0.5mol。
回答下列问题:
①平衡时CO的转化率为,该反应的化学平衡常数为。
②如果继续向该平衡体系中通入1.0mol的H2O(g),相同条件下反应达到新的平衡状态,则CO的转化率将(填“增大”、“减小”、“不变”),预计CO的转化率为。
③427℃时该反应的平衡常数为9.4,请结合①中的计算结果判断该反应的△H0(填“>”、“==”、“<”)。
①将浓氨水逐滴滴入装有生石灰的烧瓶中,可以制取氨气。
②取1mL 20%蔗糖溶液,加入适量稀硫酸,水浴加热约5min后,再加入少量新制的Cu(OH)2,加热,可检验蔗糖是否发生水解。
③配制一定物质的量浓度的NaCl溶液时,定容后摇匀,发现液面又低于刻度线,此时无须再加入蒸馏水。
④用小刀切取少量金属钠做实验,切剩的钠要立即放入原试剂瓶。
⑤在含I—的溶液中加入适量稀硫酸与H2O2(3%),再用酒精萃取,可以提取单质碘。
某反应中反应物与生成物有:
、
、
、
、
、
和一种未知物质
。
 (1)已知
在反应中得到电子,则该反应的还原剂是。
(1)已知
在反应中得到电子,则该反应的还原剂是。 (2)已知0.2
在反应中得到1
电子生成
,则
的化学式为。
(2)已知0.2
在反应中得到1
电子生成
,则
的化学式为。 (3)根据上述反应可推知。
(3)根据上述反应可推知。 a.氧化性:
〉
b.氧化性:
a.氧化性:
〉
b.氧化性:
 〉
〉
c.还原性:
〉
d.还原性:
 〉
〉
(4)将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子转移的方 向和数目:
向和数目: