(15分)
工业上以磷肥生产形成的副产物石膏(CaSO4·2H2O)与焦炭为原料可生产硫酸,同时可以得到硫酸钾肥料和氯化钙水合物储热材料。以下是有关的工艺流程示意图。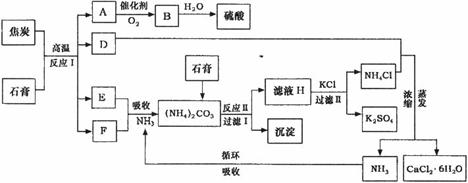
试回答:
(1)写出方程式:反应Ⅰ___________________________________,
(2)写出方程式:反应Ⅱ______________________________________。
(3)请根据下表和化学平衡知识,分析工业上制硫酸中SO2的催化氧化的适宜条件是
____________________________________。
表Ⅰ:
 压 强 / M Pa 压 强 / M Pa转化率/% 温度/℃ |
0.1 |
0.5 |
1 |
10 |
| 400 |
99.2 |
99.6 |
99.7 |
99.9 |
| 500 |
93.5 |
96.9 |
97.8 |
99.3 |
| 600 |
73.7 |
85.8 |
89.5 |
96.4 |
(4)检验滤液H中含有CO 的方法是___________________________________。
的方法是___________________________________。
(5)氯化钙结晶水合物(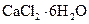 )是目前常用的无机储热材料,选择的依据是___________
)是目前常用的无机储热材料,选择的依据是___________ (填序号)。
(填序号)。
a.熔点较低(29℃熔化) b.能导电 c.易溶于水 d.无毒
【化学——物质结构与性质】太阳能电池是通过光电效应或者光化学效应直接把光能转化成电能的装置。其材料除单晶硅,还有铜铟镓硒等化合物。
(1)镓的基态原子的电子排布式是。
(2)硒为第4周期元素,相邻的元素有砷和溴,则3种
元素的第一电离能从大到小顺序为。(用元素符号表示)
(3)气态SeO3分子的立体构型为________。
(4)硅烷(SinH2n+2)的沸点与其相对分子质量的变化关系如图所示,呈现这种变化关系的原因是:__________。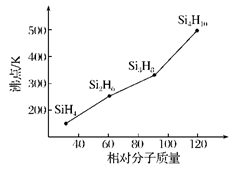
(5)与镓元素处于同一主族的硼元素具有缺电子性,其化合物往往具有加合性,因而硼酸(H3BO3)在水溶液中能与水反应生成[B(OH)4]-而体现一元弱酸的性质,则[B(OH)4]-中B的原子杂化类型为;
(6)金属Cu单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,反应的离子方程式为;
(7)一种铜金合金晶体具有面心立方最密堆积的结构。在晶胞中,Au原子位于顶点,Cu原子位于面心,则该合金中Au原子与Cu原子个数之比为__________,若该晶胞的边长为a pm,则合金的密度为_________ g·cm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)。
(15分)【化学—选修化学与技术】印尼火山喷发不仅带来壮观的美景,还给附近的居民带来物质财富,有许多居民冒着生命危险在底部的火山口收集纯硫磺块来赚取丰厚收入。硫磺可用于生产化工原料硫酸。某工厂用下图所示的工艺流程生产硫酸: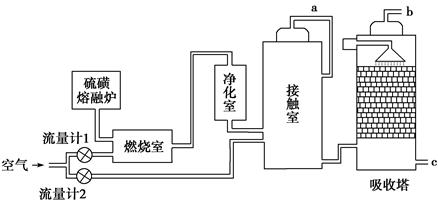
请回答下列问题:
(1)为充分利用反应放出的热量,接触室中应安装______________(填设备名称)。吸收塔中填充有许多瓷管,其作用是_____________________________________________。
(2)为使硫磺充分燃烧,经流量计1通入燃烧室的氧气过量50%,为提高SO2转化率,经流量计2的氧气量为接触室中二氧化硫完全氧化时理论需氧量的2.5倍,则生产过程中流经流量计1和流量计2的空气体积比应为________。假设接触室中SO2的转化率为95%,b管排出的尾气中二氧化硫的体积分数为__________(空气中氧气的体积分数按0.2计),该尾气的处理方法是________。
(3)与以硫铁矿为原料的生产工艺相比,该工艺的特点是________(可多选)。
A.耗氧量减少B.二氧化硫的转化率提高
C.产生的废渣减少D.不需要使用催化剂
(4)硫酸的用途非常广,可应用于下列哪些方面__________________________。
A.橡胶的硫化 B.表面活性剂“烷基苯磺酸钠”的合成
C.铅蓄电池的生产 D.过磷酸钙的制备
(5)矿物燃料的燃烧是产生大气中SO2的主要原因之一。在燃煤中加入适量的石灰石,可有效减少煤燃烧时SO2的排放,请写出此脱硫过程中反应的化学方程式______________________________。
(14分)硝酸厂废气、汽车尾气中的氮氧化物可污染大气,现有几种消除氮氧化物的方法如下:
目前,消除氮氧化物污染有多种方法。
(1)方法一:CH4催化还原法。已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH2
③H2O(g)=H2O(l) ΔH3=-44 kJ·mol-1
现有一混合气体中NO与NO2的体积比为3:1,用22.4L(标准状况下)甲烷气体催化还原该混合气体,恰好完全反应(已知生成物全部为气态),并放出1013.5KJ的热量,则ΔH2为______;写出CH4(g)与NO2(g)反应生成N2(g) 、CO2(g)和H2O(l)的热化学方程式_______________________。
(2)方法二:活性炭还原法。
某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温(T1℃)条件下反应,只生成甲和乙,甲和乙均为参与大气循环的气体,且反应进行到不同时间测得各物质的浓度如下:
 物质的量/mol 物质的量/mol时间/min |
NO |
甲 |
乙 |
| 0 |
0.200 |
0 |
0 |
| 10 |
0.116 |
0.042 |
0.042 |
| 20 |
0.080 |
0.060 |
0.060 |
| 30 |
0.080 |
0.060 |
0.060 |
由以上信息可知:
①该原理的化学方程式为____________________________________________________.
②该温度下的平衡常数K=_____________________________。(保留小数点后两位有效数字)
③若20min后升高温度至T2℃,达到平衡后,若容器中NO、甲、乙的浓度之比为1:1:1,
则该反应的ΔH_______ 0 。(填">"、"<"、"=")
(3)方法三:NH3催化还原氮氧化物(SCR技术)。该技术是目前应用最广泛的烟气氮氧化物脱除技术。
反应原理为:2NH3(g)+NO(g)+NO2(g) 2N2(g)+3H2O(g) 每生成1molN2转移的电子数为_____________________________________________________________。
2N2(g)+3H2O(g) 每生成1molN2转移的电子数为_____________________________________________________________。
(4)方法四:ClO2氧化氮氧化物。其转化流程如下: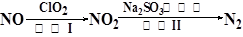
已知反应Ⅰ的化学方程式为2NO+ ClO2+ H2O = NO2+ HNO3+ HCl,则反应Ⅱ的化学方程式是。
下图所涉及的物质均为中学化学中的常见物质,其中C为空气中能够支持燃烧的气体单质、D为黄绿色气体单质、E为日常生活中最常见的金属单质,其余为化合物。它们存在如下转化关系,反应中生成的水及次要产物均已略去。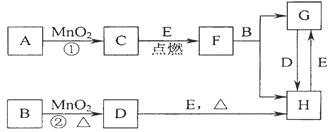
(1)写出有关物质的名称:B,F。
(2)若反应①是在加热条件下进行,则A是(填化学式);
若反应①是在常温条件下进行,则A是(填化学式)。
(3)写出B与MnO2共热获得D的离子方程式。
(10分)实验室要用12.5 mol/L的浓盐酸配制1.0 mol/L的稀盐酸100 mL。
(1)要配制上述溶液,需用量取12.5 mol/L的浓盐酸mL。
(2)配制过程中,除(1)中所选仪器、以及烧杯、玻璃棒、胶头滴管外,还需用到的仪器有。
(3)A、B是配制溶液时可能用到的二种仪器的一部分,请根据提供的情景按要求回答问题。
若按B中视线观察液面,则还需要继续进行的操作是;此操作完毕时,配制溶液的浓度(填偏高、偏低、相符)。