罗伯特·格拉布等三位科学家因在烯烃复分解反应研究方面取得了显著成就而荣获2005年诺贝尔化学奖。烯烃的复分解反应机理可视为双键断裂,换位连接,如:
CH2=CHR1 + CH2=CHR2 CH2=CH2 + R1CH=CHR2
CH2=CH2 + R1CH=CHR2
已知: F是油脂水解产物之一,能与水任意比互溶;K是一种塑料;J的化学式为C9H14O6。物质转化关系如下图所示:
请回答下列问题:
(1)请写出下列物质的结构简式:A. ▲ ,J. ▲ 。
(2)写出 C → D的化学方程式: ▲ ,该反应的反应类型是 ▲ ,
G → B的反应类型是 ▲ 。
(3)A与A的所有烯烃同分异构体之间,通过烯烃复分解反应后形成的新烯烃有 ▲ 种结构;这些新烯烃和氯化氢在一定条件下发生加成反应,则其产物只有一种结构的新烯烃的结构简式为:CH2=CH2、 ▲ 、 ▲ 。
(4)以G为原料经过一系列反应最终可制得乙酰乙酸乙酯(无色液体),通常状况下乙酰乙酸乙酯可逐渐转化为烯醇式 (达到平衡后烯醇式约占7%):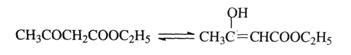
乙酰乙酸乙酯(酮式) (烯醇式)
已知FeCl3溶液可和烯醇式反应显紫色。某同学拟用5%的FeCl3溶液和Br2的CCl4溶液来证明上述平衡的存在,请简要描述实验过程和现象。
.选择下列实验方法分离物质,将分离方法的序号填在横线上。
A.萃取分液法 B 加热分解法 C.结晶法 D.分液法 E 蒸馏法 F 过滤法
(1)________分离饱和食盐水与沙子的混合的。
(2)________从KNO3和NaCl的混合溶液中获得KNO3。
(3)________分离水和汽油的混合物。
(4)________分离四氯化碳(沸点76.75℃)和甲苯(沸点110.6℃)的混合物。
(5)________从碘的水溶液里提取碘。
(6)________从NaCl与NH4HCO3固体混合物中得到NaCl。
2 mol O3和3 mol O2的质量之比________,分子数之比________,同温同压的密度之比为________,含氧原子数之比为________,体积之比为________。
Fe(OH)3胶体的制备:将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加入1mL~2mL饱和,继续煮沸至溶液呈,停止加热,即制得Fe(OH)3胶体.
反应的化学方程式: 。
如图中的①、②、③、④分别是几种常见漏斗的上部,A、B、C、D分别是实际操作时,各漏斗的下部插入容器的示意图。请根据实际使用操作时上述漏斗的使用范围和它们形状,指出①、②、③、④分别与A、B、C、D中的哪一种或几种相匹配?
①与______、②与______、③与______、④与______。
A、B、C、D、E、F、G七种物质间存在如图所示的转化关系,其中A、B、D、G含有同种元素。已知:(Ⅰ)A为金属单质; B为红褐色固体;E为密度最小的气体;G为浅绿色溶液。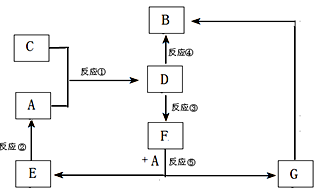
(Ⅱ)D为黄色溶液,能与硝酸银溶液反应生成不溶于稀硝酸的白色沉淀。
(Ⅲ)D能将某种氧化物氧化为F,F是含有三种元素的化合物。
请回答下列问题:
(1)上述反应中属于置换反应的是(填序号)。
(2)G生成B有多种途径。若在G的溶液中加入与G等物质的量的Na2O2,恰好使G转化为F,写出该反应的离子方程式:
反应③(即D将某种氧化物氧化为F)的离子方程式
(3)实验室制取C的化学方程式为
对气体C进行如下实验。已知整个反应过程中,每消耗0.1mol KI,转移的电子数约为3.612×1023 个。请按照要求填空:
| 实验步骤 |
实验现象 |
用化学用语解释 |
| 将少量气体通入淀粉KI溶液 |
溶液最初变成色 |
(用离子方程式表示) |
| 继续通入气体 |
溶液逐渐变成无色 |
(用化学方程式表示) |