甲、乙两种固体物质的溶解度曲线如右图所示。
(1)图中P点的含义是_____。
(2)40℃时,饱和溶液中溶质的质量分数:甲_____乙(填“>”、“=”或“<”)。20℃时,将50 g乙物质放入100 g水中,升温至40℃,溶液中溶质和溶剂的质量比为_____(用最简整数比表示)。
(3)20℃时,进行了如下图所示的实验:
①上述实验过程中属于不饱和溶液的是_____(填序号,下同),溶质的质量分数相同的是_____。
②下列操作能使E中溶液溶质的质量分数发生改变的是_____。
a.加入20 g甲 b.加入100 g水 c.升温至40℃
d.加入150 g 40℃时甲的饱和溶液,再恢复至20℃
20℃时,将等质量的甲、乙固体(不含结晶水),分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,加热到50℃时现象如图2(不考虑水分蒸发),甲、乙固体的溶解度曲线如图3.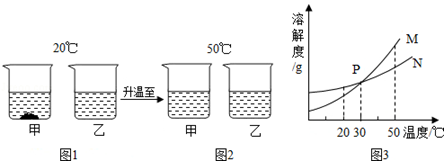
下列说法正确的是( )
| A.图1中乙溶液一定不饱和 | B.图2中两溶液中溶质质量分数一定相等 |
| C.图3中N表示甲的溶解度曲线 | D.图2中两溶液降温至30℃一定都不会析出晶体 |
根据A物质和B物质的溶解度曲线,回答下列问题: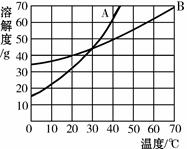
(1)20℃时,将35g A物质和35g B物质分别放入盛有100g水的烧杯中,充分搅拌,溶液达到饱和的是(填“A”或“B”)。
(2)溶解度曲线A与B的交点P的含义是。
(3)C物质的溶解度如下表,请在上图中描出C物质的溶解度曲线。
| 温度/℃ |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
| 溶解度/g |
40 |
33 |
27 |
23 |
18 |
14 |
10 |
(9分)下图是实验室中常用的几种装置,回答下列问题:
A B C D E
(1)写出有编号仪器的名称:①,②。
(2)利用上述B、C装置的组合可以制取的一种气体是;
写出制取该气体的化学方程式。
为防止生成的气体从长颈漏斗逸出,添加的液体直至。
(3)如果某同学要用氯酸钾和二氧化锰制取较纯净的氧气,选择的最佳装置是。
(4)待氯酸钾完全分解后,若想在反应后的固体中提取出氯化钾,可经过以下三个操作:
溶解 →→,便可得到少量的氯化钾固体。
煤、石油、天然气是化石燃料。
(1)石油属于(填“纯净物”或“混合物”)
(2)天然气(主要成分CH4)完全燃烧的方程式是;
(3) 煤是复杂的混合物,主要含有碳元素,还含有硫等元素,100t含硫4%的煤完全燃烧,会向空气中排放t二氧化硫。
将下列各组中的两种溶液混合(溶液中的原有的水分子忽略不写):
| 编号 |
反应物1 |
反应物2 |
混合后存在的粒子 |
| A |
稀盐酸(H+、Cl-) |
氢氧化钾溶液(K+、OH-) |
K+、Cl-、H2O |
| B |
Na+、SO42-、Cu(OH)2 |
||
| C |
氯化钠溶液(Na+、Cl-) |
稀硫酸(H+、SO42-) |
H+、SO42-、Na+、Cl- |
(1)A组发生化学变化,化学方程式为。
实质是反应物1中的(填粒子符号,下同)与反应物2中的结合形成。
(2)B组发生化学变化,且B组反应物1是盐的水溶液,反应物2是碱的水溶液,
则B组中反应物1是(填名称,下同),反应物2是;
(3)C组没有发生化学反应,原因是(微观角度解释):。