在一定体积的密闭容器中进行如下反应:
CO2(g)+H2(g)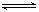 CO(g)+H2O(g);其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g);其化学平衡常数K和温度t的关系如下表:
| t℃ |
700 |
800 |
830 |
1000 |
1200 |
| K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K= 。
(2)该反应为 反应(选填“吸热”或“放热”)。
(3)能判断该反应是否达到化学平衡状态的依据是 (多选扣分)。
a.容器中压强不变 b.混合气体中c(CO)不变
c.υ正(H2)=υ逆(H2O) d.c(CO2)=c(CO)
(4)若向容器中投入各物质2mol,加热到800℃使进行反应,到达平衡时物质的量增加的物质是 。
1L某混合溶液,可能含有的离子如下表:
| 可能大量含有的阳离子 |
H+ NH4+ Al3+ K+ |
| 可能大量含有的阴离子 |
Cl- Br- I- ClO- AlO2- |
(1)往该溶液中逐滴加入NaOH溶液并适当加热,产生沉淀和气体的物质的量(n)与加入NaOH溶液的体积(v)的关系如下图所示。
则该溶液中确定含有的离子有 ;肯定不含有的离子有 ,滴加氢氧化钠过程中发生反应的先后顺序为(用离子方程式表示) 。
(2)若经检测,该溶液中含有大量的Cl—、Br—、I—,若向1L该混合溶液中通入一定量的Cl2,溶液中Cl—、Br—、I—的物质的量与通入Cl2的体积(标准状况下)的关系如下图所示,回答下列问题:
| Cl2的体积(标准状况) |
2.8L |
5.6L |
11.2L |
| n (Cl-) |
1.25mol |
1.5mol |
2mol |
| n (Br-) |
1.5mol |
1.4mol |
0.9mol |
| n(I-) |
a mol |
0 |
0 |
①当通入的Cl2的体积为2.8L时,溶液中发生反应的离子方程式为: ,a= 。
②原溶液中Cl—、Br—、I—的物质的量浓度之比为 。
高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比C12、O3、ClO2、KMnO4氧化性更强,无二次污染。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)湿法制备高铁酸钠(Na 2FeO4)的反应体系有六种微粒:Fe(OH)3、ClO—、OH-、FeO42—、Cl—、H2O。
①写出并配平湿法制备高铁酸钠的离子方程式: 。
②低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4),最可能的原因是 。
(2)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na 2FeO4+2 Na 2O+2 Na 2SO4+O2↑
该反应中的还原剂是 ,氧化产物是 ,每生成l mol Na 2FeO4转移 mol电子。
(1)下列物质中能导电的有 属于电解质的有 属于非电解质的有 。(选填字母)
A.稀硫酸
B.纯醋酸
C.铜丝
D.氨水
E.乙醇
F.硫酸钡固体
G.熔融氯化钠
H.SO3
(2)下列配制一定物质的量浓度溶液的操作中使物质的量浓度偏大的是 ,偏小的是 ,无影响的是 。(选填字母)
A.配制硫酸铜溶液时,所用的胆矾部分风化。
B.配制氢氧化钠溶液时,称量固体时间过长。
C.配制稀硫酸时,用量筒量取浓硫酸时仰视读数。
D.配制稀硫酸时,在小烧杯中稀释浓硫酸后未冷却立即转移到容量瓶中并定容。
E.转移溶液前,容量瓶内有水珠。
F.定容时,加水超过刻度线,用胶头滴管吸取液体至刻度线。
(3)用洁净的烧杯取少量蒸馏水,加热至沸腾,向烧杯中逐滴加入氯化铁的饱和溶液,可制得红褐色的胶体。
①生成该胶体的离子方程式为 。
②向该胶体中逐滴加入HI稀溶液,会出现一系列变化:先出现红褐色沉淀,随后红褐色沉淀溶解,沉淀溶解的离子方程式为 。
(共15分)利用芳香烃X和烯烃Y可以合成紫外线吸收剂BAD。已知:G不能发生银镜反应,B遇FeCl3溶液显紫色,C到D的过程为引入羧基(—COOH)的反应。其中BAD结构简式为: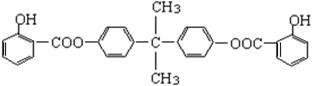
BAD的合成路线如下: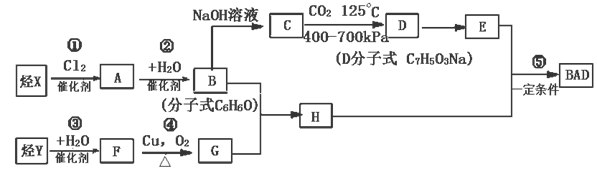
试回答下列问题:
(1)写出结构简式:Y ,D 。
(2)上述属于取代反应的有 (填数字序号)。
(3)1molBAD最多可与含 molNaOH的溶液完全反应。
(4)写出方程式
反应④ 。
B+E 。
(5)E有多种同分异构体,判断符合下列要求的同分异构体数目为 种。
①能发生银镜反应
②遇FeCl3溶液显紫色
③核磁共振氢谱图中有四个吸收峰
(共14分)SO2的含量是空气质量日报中一项重要检测指标,请结合所学知识回答下列问题。
(1)工业制硫酸过程中,SO2催化氧化的原理为:2SO2(g)+O2(g) 2SO3(g) 。T℃时,向某密闭容器中充入一定SO2(g)和O2(g),发生上述反应,测得SO2(g)的平衡转化率(a)与体系总压强(p)的关系如图所示。
2SO3(g) 。T℃时,向某密闭容器中充入一定SO2(g)和O2(g),发生上述反应,测得SO2(g)的平衡转化率(a)与体系总压强(p)的关系如图所示。
①a、b两点对应的平衡常数K(a) K(b)(填“>”、“<”或“=”,下同),SO2浓度c(a) c(b)。
②c点时,反应速率v(正) v(逆)。
(2)电化学法处理SO2。
硫酸工业尾气中的SO2经分离后,可用于制备硫酸,同时获得电能,装置如下图所示(电极均为惰性材料):
①M极发生的电极反应式为 。
②若使该装置的电流强度达到2.0A,理论上每分钟应向负极通入标准状况下气体的体积为 L(已知:1个e-所带电量为1.6×10-19C)。
(3)溶液法处理SO2。已知常温下H2SO3和H2CO3的电离常数如下表所示:
常温下,将SO2缓慢通入100mL 0.2mol•L-1的Na2CO3溶液中,当通入448mLSO2时(已折算为标准状况下的体积,下同),发生的离子方程式为 ;当通入896mLSO2时,所得溶液呈弱酸性,溶液中各离子浓度由大到小的顺序为 。