图中各物质均由常见元素(原子序数≤20)组成。已知A、B、K为单质,且在常温下A和K为气体,B为固体。D为常见的无色液体。I是一种常用的化肥,在其水溶液中滴加AgNO3溶液有不溶于稀HNO3的白色沉淀产生。J是一种实验室常用的干燥剂。它们的相互转化关系如图所示(图中反应条件未列出)。
请回答下列问题:
(1)I的化学式为 (1分); J的电子式为 (1分)
(2)F的水溶液与氯气反应的离子方程式为 (2分)
(8分)在2008年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1 mol XY2含有54 mol电子。
(1)该融雪剂的化学式是__________;X与氢元素形成的化合物的电子式是__________。
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是__________;D与E能形成一种非极性分子,该分子的结构式为__________;D所在族元素的氢化物中,沸点最低的是__________。
(3)元素W与Y同周期,其单质是原子晶体;元素Z的单质分子Z2中有3个共价健;W与Z能形成一种新型无机非金属材料,其化学式是__________。
(4)元素R与Y同主族,其氢化物能用于刻蚀玻璃,R2与NaOH溶液反应的产物之一是OR2,该反应的离子方程式为
________________________________________________________________________。
(8分)已知A、B、C、D是中学化学中常见的四种不同微粒。它们之间存在如图所示的转化关系。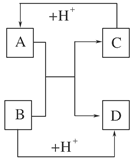
(1)如果A、B、C、D均是10电子的微粒,请写出:A的结构式________,D的电子式________。
(2)如果A和C是18电子的微粒,B和D是10电子的微粒,请写出:
①A与B在溶液中反应的离子方程式___________________________________
________________________________________________________________________。
②根据上述离子方程式,可判断C与B结合质子的能力大小是(用化学式或离子符号表示)________>________。
(3)已知肼(H2N—NH2)和甲胺(CH3—NH2)都是18个电子的分子。分析肼和甲胺的结构特点并从中受到启发,写出与其具有相同电子数的有机化合物的结构简式(至少写两个):________________________________________________________________________
________________________________________________________________________。
(8分)已知A、B、C三种元素均为第二周期非金属元素,其原子序数依次增大,且它们之间可以形成分子式为AC、BC、AC2和BC2的四种常见化合物。A、B、C可分别与氢原子形成电子总数相等的分子。
请回答下列问题:
(1)写出A、B、C三种元素的元素符号:A________,B________,C________。
(2)AC2的电子式为____________________________________________________。
(3)氢原子可以与A、B、C分别形成两组电子总数相等的分子,其电子总数分别为________和________。
(4)由1个A原子、2个B原子、1个C原子与4个氢原子构成的分子中,每个原子最外层均达到稳定结构,该分子的结构简式为________。
根据X、Y、Z、W四种常见元素的下列信息,回答有关问题:
信息1:上述四种元素均为短周期元素,其原子序数依次增大,且原子核外最外层电子数均不少于2。
(1)根据信息1,X一定不是________(填序号);
| A.氢 | B.碳 | C.氧 | D.硫 |
信息2:上述四种元素的单质均能在足量的氧气中燃烧,生成的四种氧化物中,有两种能溶于稀硫酸,三种能溶于浓氢氧化钠溶液,氧化物的相对分子质量都大于26。
(2)这四种元素中是否有一种是铝元素________(填“是”或“否”);
信息3:向上述四种元素的单质组成的混合物中加入足量稀盐酸,固体部分溶解,过滤,向滤液中加入过量的烧碱溶液,最终溶液中析出白色沉淀。
(3)生成白色沉淀物的化学式为_________________________________________;
信息4:向上述四种元素的单质组成的混合物中加入足量烧碱溶液,固体部分溶解,过滤,向滤液中加入足量的稀盐酸,最终溶液中析出白色沉淀。
(4)生成白色沉淀物的化学式为___________________________________________。
一定温度下在体积为5 L的密闭容器中发生可逆反应。
(Ⅰ)若某可逆反应的化学平衡常数表达式为: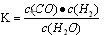
(1)写出该反应的化学方程式:;
(2)能判断该反应一定达到化学平衡状态的依据是(填选项编号)。
| A.器中气体的平均相对分子质量不随时间而变化 |
| B.υ正(H2O)=υ逆(H2) |
| C.容器中气体的密度不随时间而变化 |
| D.容器中总质量不随时间而变化 |
E.消耗n mol H2的同时消耗n mol CO
(Ⅱ)若该密闭容器中加入的是2molFe(s)与1mol H2O(g),t1秒时,H2的物质的量为
0.20mol,到第t2秒时恰好达到平衡,此时H2的物质的量为0.35mol 。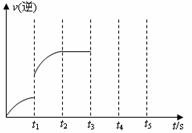
(1) t1~t2这段时间内的化学反应速率v(H2)=。
(2)若继续加入2 mol Fe(s),则平衡移动(填“向
正反应方向”、“向逆反应方向”或“不”),继续通入1mol H2O(g) 再次达到平衡后,H2物质的量为mol。
(3)该反应的逆反应速率随时间变化的关系如右图。t1时改变了某种条件,改变的条件可能是、(填写2项)