将1体积CH4和4体积Cl2组成的混合气体充入大试管中,将此试管倒立在水槽里,放在光亮处。片刻后发现试管中气体颜色 ,试管中液面上升,试管壁上出现了 ,在该反应的所有产物中(HCl除外),常温下 (填化学式)是气体,空间构型与甲烷完全相同的是 (填化学式)。试写出甲烷与氯气反应生成一氯代物的化学反应方程式 。
三氧化二铁和氧化亚铜都是红色粉末,常用作颜料。某校一化学实验小组通过实验来探究一红色粉末是Fe2O3、Cu2O或二者混合物。探究过程如下:
查阅资料
Cu2O是一种碱性氧化物, 溶于稀硫酸生成Cu和CuSO4, 在空气中加热生成CuO
提出假设
假设1:红色粉末是Fe2O3
假设2:红色粉末是Cu2O
假设3:红色粉末是Fe2O3和Cu2O的混合物
设计探究实验
取少量粉末放入足量稀硫酸中,在所得溶液中再滴加 KSCN 试剂。
(1)若假设1成立,则实验现象是。
(2)若滴加 KSCN 试剂后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁。你认为这种说法合理吗?。
(3)若固体粉末完全溶解无固体存在, 滴加 KSCN 试剂时溶液不变红色, 则证明原固体粉末是,写出所有发生的反应的离子方程式。
探究延伸
经实验分析,确定红色粉末为Fe2O3和Cu2O的混合物。
(4)实验小组欲用加热法测定Cu2O的质量分数。取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为bg( b > a),则混合物中Cu2O的质量分数为。
(5)实验小组欲利用该红色粉末制取较纯净的胆矶 (CuSO4 . 5H2O)。经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2 +、Fe2+、Fe3+分别生成沉淀的pH 如下:
| 物质 |
Cu(OH)2 |
Fe(OH)2 |
Fe(OH)3 |
| 开始沉淀pH |
6.0 |
7.5 |
1.4 |
| 沉淀完全pH |
13 |
14 |
3.7 |
实验室有下列试剂可供选择:
| A.氯水 | B.H2O2 | C.NaOH | D.Cu2(OH)2CO3 |
实验小组设计如下实验方案:
试回答:
试剂1为,试剂2为(填字母序号);固体x的化学式是。
已知A、B、C、D为常见单质,其中B、C、D常温常压下为气体,甲、乙、丙、丁为常见的化合物,乙常温下为液体,丙的焰色反应为黄色,下图为各种物质之间的转化关系。
请回答下列问题:
(1)写出下列物质的化学式:
B,D。
(2)甲的电子式为,反应②中若有11.2L(标准状况下)B生成,则发生转移的电子的物质的量为。
(3)写出反应①的离子方程式:。
写出反应③的化学方程式:。
(1)高铁酸钠(Na2FeO4)是水处理过程中的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原成三价铁离子达到净水的目的。它是由硝酸铁、氢氧化钠和氯气在一定条件下制得的,同时还生成硝酸钠和氯化钠等。
①写出制取高铁酸钠的化学方程式:;
②在制取高铁酸钠的反应中元素被氧化;
③高铁酸钠之所以有净水作用,除杀菌外,另一个原因是。
(2)在某化工厂生产中,要用到一种无色、可溶于水的晶体铝铵矾。该晶体是一种复盐,其主要化学成分为十二水合硫酸铝铵。向该复盐的浓溶液中逐滴加入浓氢氧化钠溶液。将发生一系列变化。已知,NH4+与AlO2—在水溶液中不能大量共存,会发生如下反应:NH4++A1O2—+H2O=Al(OH)3↓+ NH3↑
试回答:
①硫酸铝铵在水溶液中的电离方程式为;
②在逐滴加入浓氢氧化钠溶液的过程中,产生的现象有:a溶液中出现白色沉淀;b有刺激性气体逸出;c白色沉淀量逐渐增多;d白色沉淀完全消失;e白色沉淀逐渐减少。
请回答各种现象由先到后出现的顺序是(用序号回答):。
③并在下图中画出氢氧化钠的加入体积与沉淀量的关系.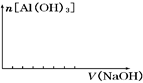
多原子分子氰(CN)2、硫氰(SCN)2和(OCN)2的性质与卤素单质相似,故称它们为拟卤素。它们可以生成酸和盐(见下表,表中X代表F、Cl、Br或I)。
| 卤素 |
氰 |
硫氰 |
① |
|
| “单质” |
X2 |
(CN)2 |
(SCN)2 |
(OCN)2 |
| 酸 |
HX |
HCN |
② |
HOCN |
| 盐 |
KX |
KCN |
KSCN |
③ |
(1)在表中①②③空格处应分别填写_______、、_______。
(2)完成下列反应的化学方程式或离子方程式。
①(CN)2和KOH溶液反应的化学方程式为:。
②已知阴离子的还原性强弱为:Cl-<Br-<CN—<SCN-<I-。试写出在NaBr和KSCN的混合溶液中加入(CN)2反应的离子方程式:____________________________________。
写出下列过程的离子方程式。
⑴除去铁粉中混有的铝粉
⑵除去CO2中混有的HCl
⑶NaAlO2溶液中通入少量CO2
⑷1 mol/L 100 mL FeBr2溶液中通入2.24 L Cl2(标准状况)