Ⅰ.由铜片、锌片和足量稀H2SO4组成的原电池中,若锌片只发生电化学腐蚀,一段时间后某极产生3.36 L(标准状况)的气体。问: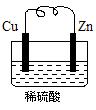
(1)负极是 (填“锌”或“铜”),发生 反应(填“氧 化”或“还原”)。
(2)正极的电极反应为
(3)产生这些气体共需转移电子 mol。
Ⅱ.氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,附气体的能力强,性质稳定,请回答: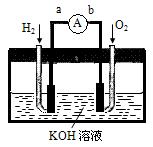
(1)氢氧燃料电池的能量转化主要形式是 ,在导线中电子流动方向为 (用a、b表示)。
(2)负极反应式为 。
(3)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一金属锂是一种重要的储氢材料,吸氢和放氢原理为: Ⅰ.2Li+H2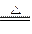 2LiH Ⅱ.LiH+H2O===LiOH+H2↑
2LiH Ⅱ.LiH+H2O===LiOH+H2↑
反应Ⅰ中的还原剂是 ,反应Ⅱ中的氧化剂是 。
某微粒的结构示意图为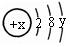 试回答:
试回答:
(1)当x-y=10时,该粒子为(选填“原子”或“阳离子”、“阴离子”);
(2)当y=8时,该粒子可能是(用化学式表示,任填3种)、、;
(3)请写出工业上制取y=7元素对应单质时的离子方程式:
。
冶炼金属常用以下几种方法:①以C、CO或H2做还原剂②以活泼金属Na、Mg等还原③利用铝热反应原理还原④电解法⑤热分解法。下列金属各采用哪种方法还原最佳。(用序号填写下列空白。)(共10分)
(1)Fe、Zn、Cu等中等活泼金属。
(2)Na、Mg、Al等活泼或较活泼金属。
(3)Hg、Ag等不活泼金属。
(4)V、Cr、Mn、W等高熔点金属。
(5)K、Rb、Cs、Ti等金属通常还原方法是。
已知乙烯能发生以下转化:
高考资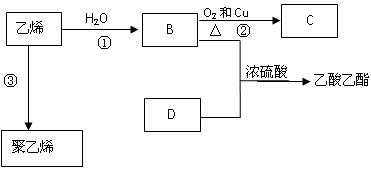
(1)乙烯的结构式为: 。
(2)写出化合物官能团的化学式及名称:
B中含官能团名称;D中含官能团名称;
(3)写出反应的化学方程式
①:反应类型:
②: 反应类型:
③:反应类型:
下图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式填空回答:
 族 族周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 二 |
① |
② |
||||||
| 三 |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
||
| 四 |
⑨ |
⑩ |
 ⑴在这些元素中,化学性质最不活泼的原子的原子结构示意图为
⑴在这些元素中,化学性质最不活泼的原子的原子结构示意图为 ⑵地壳中含量最多的金属元素是
⑵地壳中含量最多的金属元素是
⑶用电子式表示②与④形成化合物的过程 。高考资⑷这些元素中的最高价氧化物对应的水化物中,酸性最强的是 ,碱性最强的是,呈两性的氢氧化物是。
⑸写出⑤与氢氧化钠反应的化学方程式:
写出⑤的氢氧化物与氢氧化钠溶液反应的离子方程式: 。
近期石油价格暴涨,有效地利用现有能源和开发新能源已受到各国的普遍重视。
(1)可用改变汽油组成的办法来改善汽油的燃烧性能,例如加入CH3OC(CH3)3生产“无铅汽油”。CH3OC(CH3)3分子中必存在的原子间的连接形式有_______(填写编号)。



(2)天然气的燃烧产物无毒、热值高、管道输送方便,将成为我国西部开发的重点之一,天然气常和石油伴生,其主要成分是__________。能说明它是正四面体而非正方形平面结构的理由是___________(填写编号)
①其一氯代物不存在同分异构体②其二氯代物不存在同分异构体
③碳原子与氢原子之间以共价键结合④ 4个碳氢键是完全等价的
(3)1980年我国首次制成一辆燃氢汽车,乘员12人,以每小时50 km的速度行使了40km。为了有效发展民用氢能源,首先必须制得廉价的氢气。下面可供开发又较经济的制氢方法是_______________(填写编号)。
①电解水②锌与稀硫酸反应③光解海水
制得氢气后还需要解决的问题是_________________________(写出其中一个)。