如图甲乙丙三个烧杯依次分别盛放氢氧化钠溶液、硫酸铜溶液、硫酸钾溶液,电极均为石墨电极,通电一段时间,乙中c电极质量增加64克,据此回答问题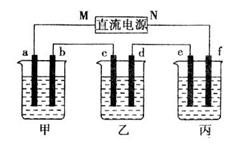
①电源的N端为 ___________极
②电极b上发生的电极反应为__________________________________
③电极b上生成的气体在标准状况下的体积______________________升
④电极e上生成的气体在标准状况下的体积_______________________升
、现有下列5种气体:Cl2、CO2、SO2、NO2、NH3。试回答下列问题:
(1)超市商品琳琅满目,但摆放和布置都清晰有序,这是因为事先进行了分类处理。
对物质进行分类是我们学习和研究化学时常用的方法,采用不同的分类标准,可以对同一组物质进行不同的分类,请你填写下表:
| A组 |
B组 |
C组 |
D组 |
|
| 分类标准 |
易溶于水 |
有毒气体 |
||
| 不属于该类别的物质 |
Cl2、NO2 |
Cl2 |
(2)Cl2是一种有毒的物质,如果发生Cl2泄漏,你将采取怎样的措施?(写一条即可)
(3)管道工人曾经用浓氨水检验氯气管道是否漏气,已知能发生如下反应(在有水蒸气存在的条件下):2NH3+3Cl2=6HCl+N2,如果氯气管道某处漏气,用该方法检查时会出现的现象是_______________________
以下是元素周期表的一部分,根据给定的元素回答下列问题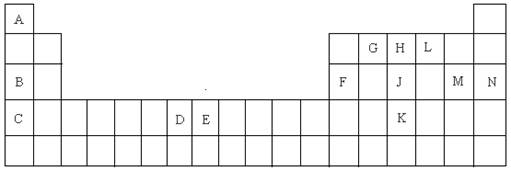
(1)K的元素符号是;
(2)D元素的外围电子排布图是,在其化合物中,最高正价是;
(3)C元素的原子结构示意图是;
(4)A与L、B与L都分别能形成原子个数比为1:1的化合物,A与L(1:1)的化合物是分子(填极性或非极性),B与L(1:1)的化合物的电子式是;
(5)G、H、L原子的第一电离能由高到低的顺序是(填元素符号);
(6)J单质的一种白色同分异构体的空间构型是;
(7)E元素在元素周期表中的位置是,在其化合物中,常有+2、+3价的2种离子,+3的离子比较稳定,其原因是;
(8)A与B的化合物的熔点比A与L的化合物的熔点高,其原因是;
(9)A的单质与L的单质与B的最高价氧化物的水化物溶液能组成燃烧电池,写出该种电池的负极的电极反应式;
(10)F元素的最高价氧化物与M元素的最高价氧化物的水化物反应的化学方程式是
。
向2 L的密闭容器中加入一定量的A、B、C三种气体,一定条件下发生反应,各物质的物质的量随时间变化如图甲所示。图乙为t2时刻后改变条件平衡体系中反应速率随时间变化的情况,且4个阶段所改变的外界条件均不相同,已知t3——t4阶段为使用催化剂。观察下图,回答下列问题: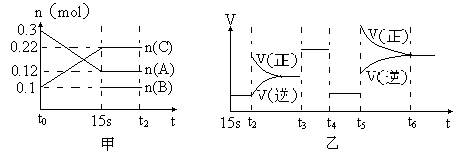
(1)甲图中从反应至达到平衡状态,生成物C的平均反应速率为。
(2)乙图中t2时引起平衡移动的条件是,t5时引起平衡移动的条件是。
(3)乙图中表示平衡混合物中,在这4个阶段中C的含量最高的一段时间是。
(4)该反应的化学方程式可以表示为:,正反应为(填“放热”或“吸热”)反应。
(5)反应开始时加入的B的物质的量为。
(1)甲烷是一种高效清洁的新能源,0.25mol甲烷完全燃烧生成液态水时放出222.5KJ热量,则甲烷燃烧的热化学方程式为_________________________。
(2)能证明甲烷是正四面体结构的理由是
①中心原子C采取sp3杂化,②中心原子C上没有孤对电子,
③CH2Cl2不存在同分异构体,④键角是109028,,而不是900
在原子结构理论中,有四个原理,分别是①构造原理,②泡利原理,③洪特规则,④能量最低原理。在以下的现象中主要决定的因素是(填序号,各只填一项)
(1)各能级最多容纳的电子数是该能级原子轨道数的2倍;
(2)碳原子的核外电子排布基态时是1s22s22p2而不是1s22s12p3;
(3)最外层电子数不会超过8个,次外层电子数不会超过18个;
(4)铬(24Cr)的电子排布式是1s22s22p63s23p63d54s1而不是1s22s22p63s23p63d44s2;
(5)磷原子的基态原子结构中,有3个未成对的单电子。