.下表标出的是元素周期表的一部分元素,回答下列问题
| 1 |
a |
|
|
||||||
| 2 |
|
|
|
|
b |
c |
d |
e |
|
| 3 |
f |
|
g |
h |
|
|
i |
j |
(1)表中列出的10种元素中,化学性质最不活泼的是___________(填元素名称,下同),
非金属性最强的是___________,原子半径最小的是___________。
(2)分子bd2的电子式______________,元素e的负一价阴离子的结构示意图_________________。
(3)物质bd2和hd2在物理性质上有着巨大差异,其原因是物质bd2属于_________________晶体,物质hd2属于______________晶体。
(4)元素e的气态氢化物比元素i的气态氢化物_________(填“稳定”或“不稳定”)
(5)元素f、g的最高价氧化物对应水化物之间反应的离子方程式是_________________________;
(6)物质fda含有的化学键类型是________________________________
按要求完成下列问题
(1)某高分子有机物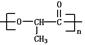 是由一种单体缩聚而成的,该单体的结构简式为。
是由一种单体缩聚而成的,该单体的结构简式为。
(2) 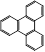 的一氯取代物有种。
的一氯取代物有种。
某混合物的水溶液中,只可能含有以下离子中的若干种:K+、Mg2+、Fe3+、Al3+、NH4+、Cl-、CO32-和SO42-。现每次取10.00mL进行实验:
①第一份加入AgNO3溶液有沉淀产生;
②第二份加入足量NaOH后加热,收集到气体0.672L(标准状况下)
③第三份加入足量BaCl2溶液后得干燥沉淀6.63g,沉淀经足量盐酸洗涤,干燥后剩余4.66g。
请回答:
⑴.c(CO32-)=______。
⑵.K+是否存在?_____________;若存在,浓度范围是__________(若不存在,则不必回答第2问)。
⑶.根据以上实验,不能判断哪种离子是否存在?若存在,这种离子如何进行检验?______、__________。
现有A、B、C、D四瓶溶液,它们分别是NaCl(0.1mol∙L-1)、HCl(0.1mol∙L-1)、NaOH(0.1mol∙L-1)和酚酞试液(0.1%)中的一种。有人不用其他试剂,就可以把它们一一鉴别开来,其实验步骤如下:
①各取溶液少许两两混合,据现象不同分成两组;
②取一组混合液,不断滴入另一组的一种未知溶液,根据现象不同可鉴别出A和B两种溶液;
③再取已鉴别出A溶液2mL, 滴入3滴未知C溶液,再加入D溶液4mL,在这个过程中无明显颜色变化;
综合以上实验可知,A、B、C、D溶液分别是:
A; B; C; D。
(每空2分共16分)20世纪50年代科学家提出价层电子对互斥模型(简称VSEPR模型),用于预测简单分子立体结构。其要点可以概括为:
Ⅰ、用AXnEm表示只含一个中心原子的分子组成,A为中心原子,X为与中心原子相结合的原子,E为中心原子最外层未参与成键的电子对(称为孤对电子),(n+m)称为价层电子对数。分子中的价层电子对总是互相排斥,均匀的分布在中心原子周围的空间;
Ⅱ、分子的立体构型是指分子中的原子在空间的排布,不包括中心原子未成键的孤对电子;Ⅲ、分子中价层电子对之间的斥力主要顺序为: i、孤对电子之间的斥力>孤对电子对与共用电子对之间的斥力>共用电子对之间的斥力; ii、双键与双键之间的斥力>双键与单键之间的斥力>单键与单键之间的斥力; iii、X原子得电子能力越弱,A-X形成的共用电子对之间的斥力越强; iv、其他。
请仔细阅读上述材料,回答下列问题:
(1)根据要点I可以画出AXnEm的VSEPR理想模型,请填写下表:
| n+m |
2 |
|
| VSEPR理想模型 |
正四面体 |
|
| 价层电子对之间的理想键角 |
109°28′ |
(2)请用VSEPR模型解释CO2为直线型分子的原因。
(3) H2O分子的立体构型为:,请你预测水分子中∠H-O-H的大小范围为,原因是。
(4) SO2Cl2和SO2F2都属AX4E0型分子,S=O之间以双键结合,S-Cl、S-F之间以单键结合。请你预测 SO2Cl2和SO2F2分子的立体构型:。
(每空1分共10分) A、B、C、D是四种短周期元素,E是过渡元素。A、B、C同周期,C、D同主族,A的原子结构示意图为: ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。
回答下列问题:
(1)用元素符号表示D所在周期(除稀有气体元素外)第一电离能最大的元素是__________,电负性最大的元素是__________。
(2) D的氢化物比C的氢化物的沸点_____(填"高"或"低"),原因____________。
(3)E元素在周期表的位置是。
(4)画出D的核外电子排布图_________________________________________,这样排布遵循了原理、____________原理和____________规则。
(5)用电子式表示B的硫化物的形成过程:______________________________。