A、B、C、D四种芳香族化合物都是某些植物挥发油中的主要成分,有的是药物,有的是香料。它们的结构简式如下所示: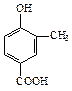
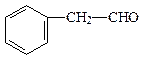
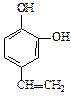
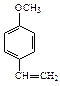
A B C D
回答下列问题:
(1)A中的含氧官能团名称是
(2)B与足量氢气充分反应的产物的结构简式为
(3)化合物C的分子式为 ,1 mol该物质完全燃烧需消耗 mol O2
(4)D发生聚合反应的产物的结构简式为
(5)A能与乙醇发生反应生成一种有特殊香味的物质,请写出该反应的方程式:
(6)关于上述四种物质的说法中正确的是
A.都能与Na反应放出H2
B.C、D均能使溴的四氯化碳溶液褪色
C.A和C均能与NaHCO3溶液反应放出CO2
D.1molC最多能与4molBr2发生反应
工业上主要采用电解饱和食盐水的方法来制取Cl2、H2、NaOH。请回答下列问题:
(1)在电解过程中,所发生反应的离子反应方程式为:;
(2)电解之前食盐水需要精制,目的是除去粗盐的中的Ca2+、Mg2+、SO42-等杂质离子,使用的试剂有:a、Na2CO3溶液 b、Ba(OH)2溶液 c、稀盐酸。其中合理的加入顺序为(填写序号) ;
(3)如果在容积为10L的电解池内,一段时间后共收集到11.2L(标准状况)气体。这时溶液中NaOH的物质的量浓度为(设电解时溶液的体积不变)。
在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;当溶液中的原有溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量、电极增重1.6g。请回答下列问题: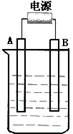
(1)A接的是电源的极,B是该装置。
(2)写出电解时反应的总离子方程式。
(3)电解后溶液的pH为;要使电解后溶液恢复到电解前的状态,则需加入,其质量为。(假设电解前后溶液的体积不变)
已知在298K时下列反应的反应热为:
(1)CH3COOH(l) + 2O2(g)=2CO2(g)+2H2O (l) △H1=-870.3KJ/mol
(2)C(s)+O2(g)=CO2(g) △H2=-393.5KJ/mol
(3)H2(g)+1/2O2(g)=H2O (l)△H3=-285.8KJ/mol
试计算下述反应的反应热:
2C(s) +2H2(g) +O2(g) =CH3COOH(l)
根据事实,写出298K时下列反应的热化学方程式:
(1)1mol氮气与适量氢气起反应,生成2mol氨气,放热92.2KJ热量。
(2)1mol碳与适量水蒸气完全反应,生成一氧化碳气体和氢气,吸收131.3KJ热量。
在298K时,热化学方程式:2H2(g)+O2(g)=2H2O (l)△H=-571.6KJ/mol 表示的意义是______________________________________;H2(g)+1/2O2(g)=H2O (l)△H=_______。