有人设计一个Na 2O 2与CO 2反应实验装置图如下:
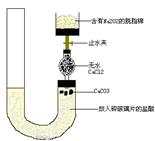
打开止水夹,发现CO 2通过裹有Na 2O 2的脱脂棉,可观察到脱脂棉剧烈燃烧起来.
(1)由实验现象所得出的有关Na 2O 2与CO 2反应的结论是:
a:有氧气生成:b:
(2)甲、乙两位同学各称取质量为m g的过氧化钠与二氧化碳反应后的样品,并用下图所示仪器测定样品的组分。

请回答下列问题:
①甲同学通过实验测得的数据是氧气的体积,该同学读取实验数据时应注意冷却至室温、____________、眼睛视线与凹液面最低处相切。
②乙同学通过连接仪器①②进行实验,他测得的数据是 。按他测得的数据计算出的实验结果偏高,理由是 。
③为了测得准确的实验数据,请你将乙同学的实验装置进行改进(每种仪器只准使用一次),写出各仪器接口  的连接顺序 。k+s-5#u
的连接顺序 。k+s-5#u
④按③设计的实验装置进行实验,若测得实验前后装置②的质量分别是w 1g和w 2g,则样品中碳酸钠的质量分数为 。
⑤在③的改进装置中由于受到仪器的局限,是否也有不足之处 (若没有,此空不必回答;若有,请一并说出不足的理由)  。
。
纯碱在工业上非常重要。
(1)取一定量纯碱细小粉末置于烧杯中,加入一定量的水,可以得到颗粒较大的晶体A。烧杯温度升高,理由是;
(2)从上述烧杯中得到干燥纯净的晶体A,实验程序为:;(填序号,可重复使用)
①蒸发结晶②放入干燥器③转移入过滤器中④用水洗涤2-3次⑤用乙醇洗涤⑥加热灼烧
(3)取纯净物13.92g晶体A,进行热重分析,直到质量不再改变,生成物质Z,具体数据如下:
| 物质 |
样品A |
T1oC下得到物质X |
T2oC下得到物质Y |
600oC时得到物质Z |
| 质量/g |
13.92 |
11.75 |
7.45 |
6.36 |
通过计算确定样品A的化学式。并写出计算过程。
某溶液中可能含有Na+,NH4+,Ba2+,SO42-,I一,SO32-中的几种,已知各离子浓度均为0.1mol/L,且溶液呈电中性。取样品分别进行实验:
①用pH试纸检测,溶液显弱酸性;
②加溴水,再加淀粉溶液均无明显现象;
据此推断该溶液中含有的离子为。
如图所示,A、B、C是实验室常用的三种制取气体的装置,提供的药品有:大理石、浓盐酸、稀盐酸、锌粒、二氧化锰、氯化铵、熟石灰。现欲利用这些药品分别制取NH3、Cl2、H2、CO2四种气体,试回答下列问题:
(1) ①写出利用上述有关药品制取氨气的化学方程式:_____________;用干燥剂干燥(填名称);
②制取CO2的化学方程式;
(2)①制取Cl2选用装置为__________(填序号);
②写出制取该气体反应的化学方程式;
③生成的气体先通过盛的洗气瓶,除去气体。
④用湿润的试纸验满。
⑤写出尾气吸收反应的化学方式。
某芳香族化合物与苯酚无论以何种比例混合,只要总物质的量一定,完全燃烧时所消耗的氧气和生成水的质量始终一定。试回答:
⑴这类物质的相对分子质量与苯酚的相对分子质量之差为_________的倍数(填数字)。
⑵这类物质中相对分子质量最小的物质A的分子式为C7H6O3。已知A溶液能与NaHCO3反应放出气体,且能与溴水反应。
①A可能的结构有________种。
②现取2.32g苯酚与A的混合物与50.0mL1.000mol/L的NaOH溶液充分反应后,加水至100mL。取出其中的10.0mL用0.100mol/L的HCl溶液滴定过量的NaOH,消耗20.0mL时至滴定终点。求该混合物中苯酚的质量分数________(结果保留三位有效数字)
通常用燃烧的方法测定有机物的分子式,可在燃烧室内将有机物样品与纯氧在电炉加热下充分燃烧,根据产品的的质量确定有机物的组成。下图所示的是用燃烧法
确定有机物物分子式的常用装置。
现准确称取0.6 g样品(只含C、H、O三种元素中的两种或三种),经燃烧后A管增重0.88 g,B管增重0.36g。请回答:
(1)按上述所给的测量信息,装置的连接顺序应是
D→ →F→ →;
(2)A、B管内均盛有有固态试剂,A管的作用是______________________;
(3)E中应盛装什么试剂:_______________;
(4)如果把CuO网去掉,A管重量将____________;(填“增大”、“减小”、或“不变”)
(5)该有机物的实验式为__________________;
(6)若该有机物低于16℃时是无色晶体,且能与碳酸氢钠反应。则其结构简式__________________。
(7)同温同压下若该有机物的密度是H2的30倍,且能发生银镜反应,写出其可能的结构简式_________________________