(8分)由A、B、C、D四种金属按下表中装置进行实验。
| 装置 |
 |
 |
 |
| 现象 |
二价金属A 不断溶解 |
C的质量 增加 |
A上有气 体产生 |
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是_________________________________________。
(2)装置乙中正极的电极反应式是_________________________________________。
(3)装置丙中溶液的pH________(填“变大”、“变小”或“不变”)。
(4)四种金属活泼性由强到弱的顺序是_______________________________________。
(12分)工业上用碘酸盐(碘酸为强酸)制备高碘酸(H5IO6,属于弱酸),并用高碘酸在酸性介质中氧化Mn2+生成MnO4—,其流程如下图所示:
(1)反应Ⅰ是将碘酸钠氧化为不溶于水的Na2H3IO6,该反应的化学方程式为________。
反应Ⅱ得到的是不溶于水的黑色Ag5IO6,过滤Ⅱ的滤液呈________(填“酸”、“碱”或“中”)性。
(2)无色气体的名称为________。白色滤渣的化学式为________。
(3)工业上为降低成本,减少对环境的污染,整个流程需要控制加入氯气和硝酸银的物质的量之比为n(Cl2)∶n(AgNO3)=________。
(4)氧化Mn2+过程中,消耗1 mol H5IO6时,转移2 mol电子,则该反应的离子方程式为________。
从某废触媒[主要成分为活性炭、ZnO、FeO、(CH3COO)2Zn]中制取醋酸锌晶体的实验步骤如下:
(1)浸取时,在三口烧瓶中加入废触媒及稀醋酸,给三口烧瓶加热并同时开动搅拌器的目的是。
(2)若先将废触媒在马弗炉中通氧气500℃处理一段时间,浸出率会大大提高,其原因是。抽滤时用的硅酸盐质仪器有和。
(3)流程图中加入H2O2的目的是。
(4)所得晶体(CH3COO)2Zn·2H2O热重分析(TG/%=固体样品的剩余质量/固体样品的起始质量),文献表明分解分三个阶段,在200°C以下脱去两分子结晶水,形成的(CH3COO)2Zn在242°C熔融,370°C完全分解为ZnO同时生成CO2及一种含氧衍生物(核磁共振氢谱只有1组峰)。(CH3COO)2Zn分解生成氧化锌的反应方程式为。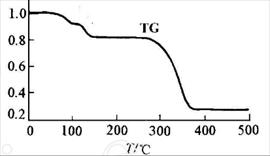
实验室用MnO2、KOH及KClO3为原料制取高锰酸钾的实验流程如下:
(1)熔融时需用铁坩埚和铁制搅拌棒而不能用玻璃仪器,其原因是。
(2)熔融时,MnO2转化为K2MnO4,KClO3转化为KCl,其反应的化学方程式为。
(3)几种物质的溶解度曲线如图所示。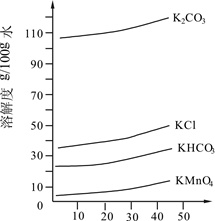
①歧化时,通入CO2至pH为10~11,K2MnO4绿色溶液转化为KMnO4和MnO2。其反应的离子方程式为。
②歧化时不能通入过量CO2的原因是。
③通入CO2后,用玻璃棒蘸取溶液点于滤纸上,观察到,证明歧化反应已发生。
④歧化后得到KMnO4晶体的操作依次为过滤、、及干燥。
(4)在此实验流程中可循环使用的物质的化学式为。
利用硫酸渣(主要含Fe2O3、FeO,杂质为Al2O3和SiO2等)生产铁基颜料铁黄(FeOOH)的制备流程如下: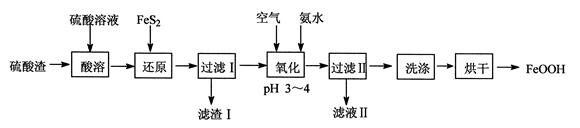
(1)“酸溶”时,Fe2O3与硫酸反应的化学方程式为。
(2)滤渣Ⅰ的主要成分是FeS2、S和(填化学式);Fe3+被FeS2还原的离子方程式为。
(3)“氧化”中,生成FeOOH的离子方程式为。
(4)滤液Ⅱ中溶质是Al2(SO4)3和(填化学式);“洗涤”时,检验铁黄表面已洗涤干净的操作是。
B.【实验化学】
水杨酸可用于制备解热镇痛药阿司匹林。重结晶纯化固体水杨酸的步骤如下:
步骤1:按图1所示装置,在圆底烧瓶中加入1.2 g粗水杨酸,10 mL 30%乙醇和磁子。接通冷凝水后,搅拌加热至沸,直到完全溶解。
步骤2:冷却后,加入活性炭,重新搅拌加热煮沸几分钟后,利用图2装置趁热过滤到锥形瓶中,并在短颈漏斗上盖好表面皿。
步骤3:盛滤液的锥形瓶用塞子塞好,自然冷却后再用冰水冷却,析出水杨酸晶体。
步骤4:用图3所示装置进行抽滤,用少量30%的乙醇洗涤。抽干后得到的晶体转移到表面皿上,放入干燥器中干燥。
步骤5:称量干燥后固体质量为0.81 g。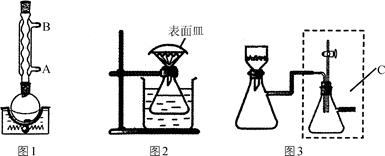
(1)步骤1中接通冷凝水时,冷水应从________(填“A”或“B”)端进。
(2)步骤2中“趁热过滤”的目的是______________________。
(3)步骤3中“自然冷却后再用冰水冷却”,而不直接用冰水浴冷却的目的是________。
(4)步骤4中C装置的作用是______________________________________。
(5)本次实验中,水杨酸的收率为________。确定最终产品是水杨酸的实验或方法是___________。