(8分)(2010·北京卷)镇痉药物C、化合物N以及高分子树脂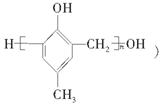 的合成路线如下:
的合成路线如下: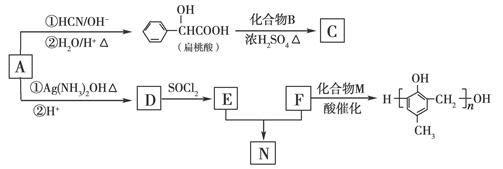
已知:
RCHO①HCN/OH-②H2O/H+△
RCOOH RCOOR′ (R、R′代表烃基)
RCOOR′ (R、R′代表烃基)
(1)A的含氧官能团的名称是________。
(2)A在催化剂作用下可与H2反应生成B。该反应的反应类型是________。
(3)酯类化合物C的分子式是C15H14O3,其结构简式是________。
(4)A发生银镜反应的化学方程式是
________________________________________________________________________。
(5)扁桃酸(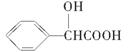 )有多种同分异构体。属于甲酸酯且含酚羟基的同分异构体共有________种,写出基中一种含亚甲基(-CH2-)的同分异构体的结构简式________。
)有多种同分异构体。属于甲酸酯且含酚羟基的同分异构体共有________种,写出基中一种含亚甲基(-CH2-)的同分异构体的结构简式________。
(6)F与M合成高分子树脂的化学方程式是________。
(7)N在NaOH溶液中发生水解反应的化学方程式是________。
膳食纤维具有的突出保健功能,近年来受到人们的普遍关注,被世界卫生组织称为人体的“第七营养素”。木质素是一种非糖类膳食纤维,其单体之一是芥子醇,结构如下图所示。
| A.芥子醇的分子式是C11H12O4,属于芳香族化合物 |
| B.芥子醇分子中所有碳原子一定在同一平面上 |
| C.芥子醇分子中含9种不同化学环境的H原子 |
| D.1mol芥子醇能与足量溴水反应消耗1molBr2 |
(6分)随着化石能源的减少,新能源的开发利用日益迫切。
(1)Bunsen热化学循环制氢工艺由下列三个反应组成:
①SO2(g)+I2(g)+2H2O(g)=2HI (g)+H2SO4(l) ΔH=a kJ·mol-1
②2H2SO4(l)=2H2O(g)+2SO2(g)+O2(g) ΔH=b kJ·mol-1
③2HI(g)=H2(g)+I2(g) ΔH=c kJ·mol-1
则:2H2O(g)=2H2(g)+O2(g)ΔH=kJ·mol-1
(2) 已知在101 kPa时,CH4完全燃烧生成1mol液态水,放出的热量为QkJ,则CH4完全燃烧反应的热化学方程式是:。
(3)1molN2(g)和1molO2(g)在一定条件下反应生成2molNO(g),吸收180kJ的热量,已知断裂1molN2(g)中的N≡N和1molO2(g)中的O=O分别需要吸收946kJ和498kJ的能量,则1molNO分子中的化学键形成时可释放kJ的能量。
元素周期表是学习物质结构与性质的重要工具。下表是元素周期表的一部分,表中所列字母A、B、D、E、G、H、Q、M、R分别代表某一化学元素。请用所给元素回答下列问题。
| A |
|||||||||||||||||
| M |
B |
D |
|||||||||||||||
| G |
H |
Q |
R |
||||||||||||||
| E |
|||||||||||||||||
(1)Q元素在元素周期表中的位置,E元素原子结构示意图为
(2)E、Q、R三种元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是(填离子符号)_________________________________。
(3)M、D两元素形成的化合物中含有的化学键类型是,其MD2分子的结构式:
(4)用电子式表示物质GDA_________________; 用电子式表示G与Q形成化合物的过程;
(5)用表中所给元素组成反应物,请各用一个化学方程式说明元素Q和R非金属性的强弱:;元素G、H的金属性强弱:
Ⅰ、一定温度下,在容积为V L的密闭容器中进行反应:aN(g) bM(g),M、N的物质的量随时间的变化曲线如图所示:
bM(g),M、N的物质的量随时间的变化曲线如图所示: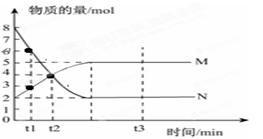
(1)此反应的化学方程式中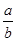 =__________
=__________
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为:
(3)平衡时,N的转化率为。
(4)下列叙述中能说明上述反应达到平衡状态的是
| A.反应中M与N的物质的量之比为1︰1 |
| B.混合气体的总质量不随时间的变化而变化 |
| C.混合气体的总物质的量不随时间的变化而变化 |
| D.单位时间内每消耗a mol N,同时生成b mol M |
E.混合气体的压强不随时间的变化而变化F.N的质量分数在混合气体中保持不变
II、某研究性学习小组为探究锌与盐酸反应,取同质量、同体积的锌片、同浓度盐酸做了下列平行实验:
实验①:把纯锌片投入到盛有稀盐酸的试管中,发现氢气发生的速率变化如图所示:
实验②:把纯锌片投入到含FeCl3的同浓度工业稀盐酸中,发现放出氢气的量减少。
实验③:在盐酸中滴入几滴CuCl2溶液,生成氢气速率加快。
试回答下列问题:
(1)试分析实验①中t1~t2速率变化的主要原因是,t2~t3速率变化的主要原因是。
(2)实验②放出氢气的量减少的原因是。
(3)某同学认为实验③反应速率加快的主要原因是因为形成了原电池,你认为是否正确?
(填“正确”或“不正确”)。请选择下列相应的a或b作答。
a、若不正确,请说明原因:
b、若正确则写出实验③中原电池的正极电极反应式。
在一容积为2L的密闭容器中加入2molA和6molB,保持温度为20℃,在催化剂存在的条件下进行下列反应:A(g)+2B(g)  2C(g),达平衡后生成1.2mol C,平衡混合气体中C的体积分数为ω。
2C(g),达平衡后生成1.2mol C,平衡混合气体中C的体积分数为ω。
(1)求20℃时,该反应的平衡常数K(保留三位有效数字)
(2)20℃时,若在同一容器中加入1molA、mol B和mol C,则平衡混合气中C的体积分数仍为ω。