将2.4mol某金属投入1.8L 2mol/L的盐中,恰好完全反应,并得到7.2gH2,则某金属的化合价为 ,酸为 元酸。
含苯酚的工业废水的方案如下图所示: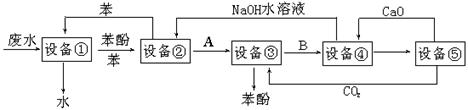
回答下列问题:
⑴设备①进行的是操作(填写操作名称),实验室这一步操作所用的仪器是;
⑵由设备②进入设备③的物质A是,由设备③进入设备④的物质B是;
⑶在设备③中发生反应的化学方程式为;
⑷在设备④中,物质B的水溶液和CaO反应,产物是、和水,可通过操作(填写操作名称)分离产物;
⑸上图中,能循环使用的物质是C6H6、CaO、、。
现有下列5种有机化合物:
| A.CH3OH | B.(CH3)3CCH2OH | C.(CH3)3COH | D.(CH3)2CHOH |
E、C6H5CH2OH
(1)能氧化成醛的是。
(2)不能消去成烯的是。
(3)能氧化成酮的是。
图中A、B、C、D、E、F、G均为有机化合物。
根据上图回答问题。
(1)D的化学名称是。
(2)反应③的化学方程式是。
(3)B的分子式是。A的结构式是。
反应①的反应类型是。
(4)符合下列3个条件的B的同分异构体数目有个。
①含有邻二取代苯环结构②与B有相同官能团③不与FeCl3溶液发生显色反应
写出其中任意一种同分异构体的结构简式。
(5)G是重要的工业原料,用化学方程式表示G的一种重要工业用途:。
有下列各组物质:
| A.O2和O3; | B. U和 U和 U; U; |
C.CH3CH2CH2CH3和 ; ; |
D. (E)甲烷和新戊烷 (E)甲烷和新戊烷 |
(1)___组两物质互为同位素; (2)___组两物质互为同素异形体;
(3)___组两物质互为同系物; (4)___组两物质互为同分异构体;
(5)___组两物质互为同一物质。
把1.0 mol X和1.0 mol Y气体混合于2 L的密闭容器中,发生如下反应 2X(g)+Y(g)  nZ(g)+2W(g)2min末,生成0.4 mol W,以Z的浓度表示的反应速率为0.1mol/(L·min)
nZ(g)+2W(g)2min末,生成0.4 mol W,以Z的浓度表示的反应速率为0.1mol/(L·min)
(1)前2min以X的浓度表示的平均反应速率为
(2)2min末时Y的浓度为
(3)n=