下图所示装置是用于气体制备、干燥、性质验证、尾气处理的部分仪器装置(加热及夹持固定装置均已略去)。请根据下列要求回答问题。
(1)若烧瓶中盛装Zn片,分液漏斗中盛装稀H2SO4,则:
①当制备H2、验证H2的还原性并检验H2的氧化产物,仪器连接顺序为:A→C→B
→B→D时,两次使用B装置,其中所盛的药品依次是 、
(写化学式);D装置的作用是
。
②上述实验中为了使H2产生的速率不至于过快,在不改变现有药品的条件下,可采取的方法有 、
。(要求:写出的两种方法原理不同)
(2)若烧瓶中盛装Na2O2,分液漏斗中盛装浓氨水,则:
①烧瓶内除了能产生O2外,还能产生大量NH3。能产生大量NH3的原因是:
a ;b ;c 。
②用产生的气体做氨的催化氧化实验,各仪器装置按气流方向(从左到右)连接顺序是:A→ → → (填正确序号的字母)此时在其中的一个装置中可能会出现大量红棕色气体,该装置是 (用字母表示);用化学方程式解释红棕色气体产生的原因: 、
。
聚合硫酸铁又称聚铁,化学式为[Fe2(OH)n(SO4)3-0.5n]m,广泛用于污水处理。实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁和绿矾(FeSO4·7H2O),过程如下:
(1)验证固体W焙烧后产生的气体含有SO2的方法是:
___________________________________________________________________。
(2)实验室制备、收集干燥的SO2,所需仪器如下。装置A产生SO2,按气流方向连接各仪器接口,顺序为a→____→____→____→____→f。
装置A中发生反应的化学方程式为_________________________________________。
装置D的作用是_____________,装置E中NaOH溶液的作用是__________________。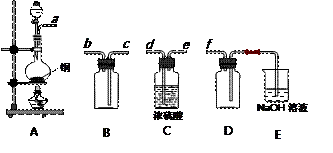
(3)制备绿矾时,向溶液X中加入过量__________,充分反应后,经过滤操作得到溶液Y,再经浓缩、结晶等步骤得到绿矾。过滤所需的玻璃仪器有_______________________。
(4)欲测定溶液Y中Fe2+的浓度,需要用容量瓶配制KMnO4标准溶液,定容时视线应_____________________,直到_____________________。用KMnO4标准溶液滴定时应选用________滴定管(填“酸式”或“碱式”)。
(5)溶液Z的pH影响聚铁中铁的质量分数。若溶液Z的pH偏小,将导致聚铁中铁的质量分数______(填“偏大”、“偏小”或“无影响”)。
某化学课外小组为了探究CaCl2溶液和Na2SO4溶液反应有没有限度,设计了如下活动过程,请完成表中空格:(已知CaSO4在水中微溶,CaCO3在水中难溶)
| 实验步骤 |
向3—4 mL 1 mol/L的CaCl2溶液中滴入1mol/L的Na2SO4溶液至反应完全 |
| 实验现象 |
产生白色沉淀 |
| 离子方程式 |
(1) |
| 小组讨论交流 |
向上述反应后的清液中滴入适量1mol/L的Na2CO3溶液会出现什么现象 |
| 假设出现的实验现象,说明理由 |
假设:Ⅰ无现象 理由:反应没有限度,Ca2+沉淀完全 假设:Ⅱ(2),理由:(3) |
| 证明你的假设 |
现象:产生大量的白色沉淀 |
| 离子方程式 |
(4) |
| 解释 |
(5) |
某化学兴趣小组为了探究:在常温下某非金属氧化物形成的未知气体的成分。该小组成员将气体通入澄清石灰水,发现澄清石灰水变浑浊,持续通入发现浑浊又变澄清,由此该小组成员对气体的成分提出猜想。
[提出猜想]
猜想1:;猜想2;猜想3。
为了验证猜测,该小组设计实验加以探究:
[实验探究]
该小组同学按如图所示装置,将气体从a端通入: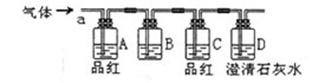
(1)B中应该装下列试剂(填编号);
| A.NaCl溶液 | B.KMnO4溶液 | C.浓溴水 | D.饱和NaHCO3溶液 |
(2)A中品红的作用是:;
(3)D中澄清石灰水的作用是:。
通过该实验,小组同学观察到以下三个实验现象:
①A中品红褪色②C中品红不褪色③D中澄清石灰水变浑浊
[得出结论]
由上述现象小组同学确认该气体的成分是。
实验室用98%的浓硫酸(其密度为1.84 g/ml)配制100 mL
1.0 mol·L-1稀硫酸。
(1)需用10 mL的量筒量取浓硫酸的体积为mL。
(2)实验时选用的仪器有10 mL量筒、烧杯、玻璃棒、、。
(3)配制过程中,下列情况会使配制结果偏低的是(填序号)。
A.用量筒量取浓硫酸时,仰视量筒的刻度
B.转移液体到容量瓶中时,未洗涤烧杯就定容
C.往容量瓶转移时,有少量液体溅出
D.容量瓶使用时未干燥
E.定容时俯视刻度线观察液面
(4)在容量瓶使用方法中,下 列操作正确的是(填序号)。
列操作正确的是(填序号)。
A.容量瓶用蒸馏水洗净后,再用待配液润洗
B.使用容量瓶前检查它是否漏水
C.将氢氧化钠固体放在天 平托盘的滤纸上,准确称量并放入烧杯中溶解后,立即注入容量瓶中
平托盘的滤纸上,准确称量并放入烧杯中溶解后,立即注入容量瓶中
D.将准确量取的18.4 mol·L-1的硫酸,注入已盛有30 mL水的100 mL的容量瓶中,加水至刻度线
mol·L-1的硫酸,注入已盛有30 mL水的100 mL的容量瓶中,加水至刻度线
(4分)下图是实验室制取溴苯的装置:
导管a段的作用。反 应后不久导管b出口可见到白雾,导管b段末端跟锥形瓶里液面保持一段距离的目的是___________________。
应后不久导管b出口可见到白雾,导管b段末端跟锥形瓶里液面保持一段距离的目的是___________________。