几种中学化学常见的单质及其化合物相互转化的关系图如下: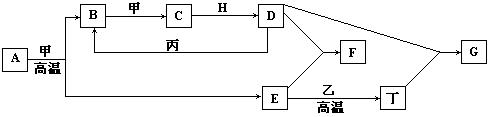
可供参考的信息有:
①甲、乙、丙、丁为单质,其余为化合物。
②A由X和Y两种元素组成,其原子个数比为1:2,元素质量之比为7:8。
③B气体是引起酸雨的主要物质,H常温下为无色 无味的液体,E为红棕色固体,常用作油漆和涂料。试根据上述信息回答下列问题:
无味的液体,E为红棕色固体,常用作油漆和涂料。试根据上述信息回答下列问题:
(1)A的化学式为 ;
(2)F与丁单质也可以化合生成G,试写出该反应的离子方程式:
(3)少量F的饱和溶液与分别滴加到下列物质中,得到三种分散系①、②、③。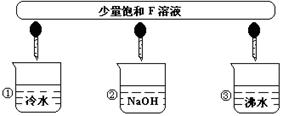
试将①、②、③填入下列方框中: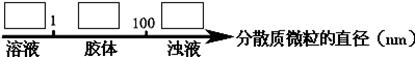
(4)化合物M与H组成元素相同,可以将G 氧化为F,且不引进新的离子。试写出M在酸性环境下将G氧化为F的离子方程式:
氧化为F,且不引进新的离子。试写出M在酸性环境下将G氧化为F的离子方程式: 
汽车内燃机工作时产生的高温会引起N2和O2的反应:N2(g)+O2(g) 2NO(g),是导致汽车尾气中含有NO的原因之一。某同学为控制污染,对该反应进行研究。
2NO(g),是导致汽车尾气中含有NO的原因之一。某同学为控制污染,对该反应进行研究。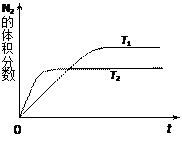
⑴右图表示在T1、T2两种不同温度下,一定量的NO发生分解过程中N2的体积分数随时间变化的图像,根据图像判断反应N2(g)+O2(g) 2NO(g)为(填“吸热”或“放热”)反应。
2NO(g)为(填“吸热”或“放热”)反应。
⑵2000℃时,向容积为2L的密闭容器中充入10molN2与5mol O2,达到平衡后NO的物质的量为2mol,则2000℃时该反应的平衡常数K=。该温度下,若开始时向上述容器中充入N2与O2均为1 mol,则达到平衡后N2的转化率为。
⑶为避免汽车尾气中的有害气体对大气的污染,给汽车安装尾气净化装置。净化装置里装有含Pd等过渡元素的催化剂,气体在催化剂表面吸附与解吸作用的机理如下图所示。
写出上述变化中的总化学反应方程式:。
某研究性学习小组为测定镁和铝的混合物中铝的质量分数,称取该混合物a g,溶于200 mL 5 moL HCl溶液中,共收集到标准状况下的氢气3.36 L。
(1)a的取值范围是 _______ 。
(2)向反应后所得溶液中逐渐加入4 mol/L的NaOH溶液。当沉淀质量达到最大值时,加入的NaOH溶液的体积是 _______ mL,沉淀的最大质量是 _______ g(用含a的代数式表示)
(3)继续加入NaOH溶液至沉淀质量不再发生变化时,过滤、洗涤并灼烧沉淀至恒重,所得残余固体的质量仍为a g,计算原混合物中铝的质量分数(写出计算过程)。
A.《物质结构与性质》
(1)前三周期元素中第一电离能最小的是 _______(填元素符号),其基态原子的电子排布式为 _______。第二周期非金属元素形成的氢化物中化学键极性最大的是 _______
(填分子式),该物质在CCl4中的溶解度比在水中的溶解度 _______(填“大”或“小”)。
 |
(2)物质形成分子间氢键和分子内氢键对物质性质的影响有显著差异。根据下表数据,形成分子间氢键的物质是 _______(填物质字母代号)。
(3)晶格能的大小:MgO _______NaCl,键能的大小:HBr _______HI。(填“>”、“=”或“<”)
(4)下列物质的熔点高低顺序,正确的是 _______
A.金刚石>晶体硅>二氧化硅>碳化硅
B.CI4 > CBr4 > CCl4 > CH4
C.SiF4 > NaF > NaCl > NaBr
B《实验化学》
七水硫酸镁(MgSO4·7H2O)在印染、造纸和医药等工业上都有广泛的应用,利用化工厂生产硼砂的废渣-一硼镁泥可制取七水硫酸镁。硼镁泥的主要成分是MgCO3,还含有其他杂质(MgO、SiO2、Fe2O3、FeO、CaO、Al2O3、MnO等)。
表1部分阳离子以氢氧化物形式完全沉淀时溶液的pH
| 沉淀物 |
Al(OH)3 |
Fe(OH)3 |
Fe(OH)2 |
Mn(OH)2 |
Mg(OH)2 |
| pH值 |
5.2 |
3.2 |
9.7 |
10.4 |
11.2 |
表2两种盐的溶解度(单位为g/100g水)
| 温度 / ℃ |
10 |
30 |
40 |
50 |
60 |
| CaSO4 |
0.19 |
0.21 |
0.21 |
0.20 |
0.19 |
| MgSO4·7H2O |
30.9 |
35.5 |
40.8 |
45.6 |
/ |
硼镁泥制取七水硫酸镁的工艺流程如下: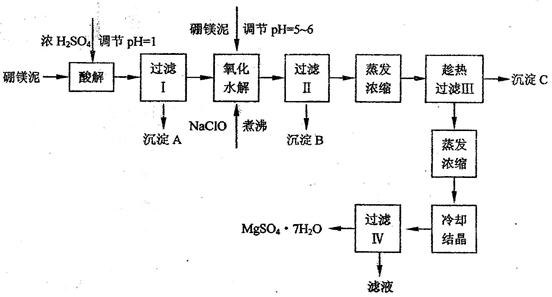
根据以上流程图并参考表格pH数据和溶解度数据,试回答下列问题:
(1)过滤I的滤液中加入硼镁泥,调节溶液的pH=5~6,再加入NaClO溶液加热煮沸,将溶液中的Mn2+氧化成MnO2,反应的离子反应方程式为 _______。加热煮沸的主要目的是_ _______。
(2)沉淀B中除MnO2、SiO2外还含有 _______(填化学式)等物质。
(3)检验过滤Ⅱ后的滤液中是否含有Fe3+的实验方法是 _______;
(4)沉淀C的化学式是 _______。过滤II需趁热过滤的理由是 _______
80年代中期美国学者Modell首次提出超临界水氧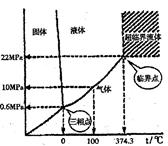
化技术(SCWO)。超临界流体(SCF)是指流体的温度和压
力处于它的临界温度(Tc)和临界压力(Pc)以上时的一种
特殊状态的流体,它具有许多独特的性质,如无机盐在超
临界水(SCW)中的溶解度很低。水的状态与压强、温度的
关系如右图。
(1)在380℃.20 MPa时,水的状态是 _______,若要使
之成为超临界水,必须采取的措施是 _______。
(2)以超临界水为介质,用氧气等氧化剂可将有机废物氧化成二氧化碳、氮气、水等无毒小分子。在超临界水中,偏二甲胼[(CH3)2NNH2]能迅速被H2O2氧化,写出该反应的化学方程式: _______
(3)SCWO基本工艺流程如下图所示: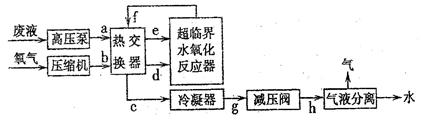
利用以上工艺流程处理某些含可溶性无机盐(只含钠盐、钾盐)的有机废水时,常常会出现管道堵塞现象,发生这种现象的原因是 _______。若检测到管道c中的流体的温度为287℃,管道e、d中的流体的温度为227℃,则上述a~h管道中易发生堵塞的管道为 _______(填字母)。
实验室用右图所示的装置制取溴乙烷。在试管I中依次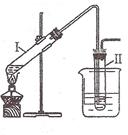
加入2 mL 蒸馏水、4 mL浓硫酸、2 mL 95%的乙醇和3g溴化钠
粉末,在试管Ⅱ中注入蒸馏水,在烧杯中注入自来水。加热试管
I至微沸状态数分钟后,冷却。
试回答下列问题:
(1)试管I中浓硫酸与溴化钠加热反应生成氢溴酸,写出氢溴酸与乙醇在加热时反应的化学方程式 _______。
(2)试管I中反应除了生成溴乙烷,还可能生成的有机物有 _______(任写两种结构简式)。
(3)设计实验证明试管Ⅱ收集的溴乙烷中含有溴元素,完成以下实验报告:
| 实验步骤 |
实验操作 |
预期现象和结论 |
| 1 |
_______ |
_______ |
| 2 |
_______ |
_______ |
| 3 |
_______ |
_______ |
| 4 |
_______ |
_______ |
(4)设计实验方案,检验溴乙烷与NaOH乙醇溶液发生消去反应后生成的气体X中是否含乙烯。在答题卡对应的方框中画出实验装置图,并注明所用试剂的名称。