(共12分)根据给出的有机物的结构简式或名称按要求填空:
①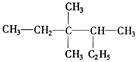 ②
②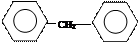 ③
③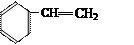
④5,5-二甲基-4-乙基-2-己炔 ⑤ ⑥
⑥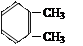
⑦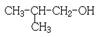

(1)写出①的系统命名法的名称 ;(2)写出④的结构简式 ;
(3)属于脂肪烃的是 (填序号);(4)属于芳香烃的是 (填序号);
(5)属于苯的同系物是(填序号);(6)任写一种与⑧ 互为同分异构体的结构简式 。
互为同分异构体的结构简式 。
某氮肥厂氨氮废水中的氮元素多以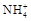 和NH3·H2O的形式存在,该废水的处理流程如下所示:
和NH3·H2O的形式存在,该废水的处理流程如下所示:
过程Ⅰ:加NaOH溶液,调节pH至9后,升温至30 ℃,通空气将氨赶出并回收a.n
过程Ⅱ:在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-。两步反应的能量变化示意图如下图: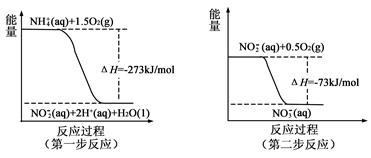
(1)第一步反应是_______________反应(选填“放热”或“吸热”),判断依据是__________。
(2)1 mol NH4+(aq)全部氧化成NO3-(aq)的热化学方程式是 。
高效净水剂聚合氯化铝铁(PAFC)的组成可表示为[AlFe(OH)nCl6-n]m,该物质广泛应用于日常生活用水和工业废水的处理。
(1)为检测PAFC中铝和铁元素的含量,采用如图所示流程进行。
回答下列问题:
①PAFC中铁元素的化合价为_________。
②步骤I中的试剂A是(从“氢氧化钠溶液”、“氨水”中选择)
步骤Ⅲ中的试剂B是。
③步骤Ⅱ的操作是,用到的主要玻璃仪器。
(2)某工厂欲以工业废料(铁、铁和铝的氧化物)为原料制取PAFC,设计如下流程:
①在废料中加入过量稀盐酸,发生多个离子反应,请在空白处补全离子方程式:
FeO+2H+ Fe2++H2O Al2O3+6H+
Fe2++H2O Al2O3+6H+ 2Al3++3H2O
2Al3++3H2O
Fe2O3+6H+ 2Fe3++3H2O
2Fe3++3H2O
②所得酸性溶液中,不能确定是否一定存在的阳离子是(填序号)。
A.Al3+ B.Fe2+ C.Fe3+ D.H+
为证明该离子确实存在,可采用的操作(必须指明所采用的试剂及观察到的现象)是:。
③往酸性溶液中加入试剂X的目的是(用离子方程式表示)。
某同学设计如下实验方案,分离KCl和BaCl2两种固体混合物。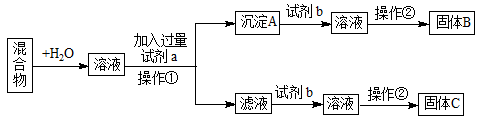
试回答下列问题:
(1)试剂a是;试剂b是;固体B是。(填化学式)
(2)操作②的名称是:、、干燥。
(3)加入试剂a所发生的离子方程式为:。
沉淀A与试剂b所发生的离子方程式为:。
已知钙的金属活泼性介于钾和钠之间,其化学性质与钠相似。钙及其化合物的有关反应如下:
①Ca+2H2O Ca(OH)2+H2↑②CaO+H2O
Ca(OH)2+H2↑②CaO+H2O Ca(OH)2
Ca(OH)2
③CaO2+H2O ④CaO+CO2
④CaO+CO2 CaCO3
CaCO3
⑤2CaO2+2CO2 2CaCO3+O2
2CaCO3+O2
结合所学知识完成下列问题:
(1)完成上述③的化学方程式: CaO2 + H2O ;
;
(2)用双线桥标出反应①的电子转移方向和数目:Ca+2H2O Ca(OH)2+H2↑
Ca(OH)2+H2↑
(3)写出以钙为原料制取过氧化钙(CaO2)的化学方程式:;
(4)在CaO2的水溶液中,滴入酚酞溶液,预期的实验现象可能是;在该溶液中加入少量的MnO2固体,有气泡生成,写出该反应的化学方程式。
Ⅰ.根据条件回答下列问题:
下图是医院病人输液使用的一瓶质量分数为5%的葡萄糖(C6H12O6)注射液标签,请认真观察标签所列内容后填写:
(1)该葡萄糖注射液属于分散系中的(从“溶液”、“胶体”、“浊液”中选择)。
(2)葡萄糖的摩尔质量为。
(3)已知该葡萄糖注射液的密度是1g/mL,其物质的量浓度为(列式计算)。
Ⅱ.钠与水反应的过程如下图所示。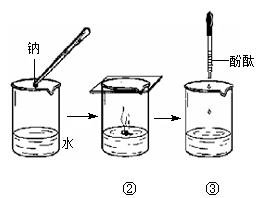
请回答:
(1)钠与水反应的化学方程式为;
(2)根据②中的实验现象,说明钠的密度比水的(填“大”或“小”)。
(3)③中滴入酚酞试液后,可观察到溶液变色。
(4)在实验室中通常将钠保存在里。