(16分)工业“从海水中提取镁”的流程图如下: 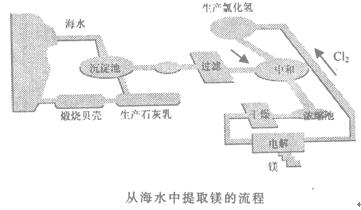
步骤为: ①将海边大量的贝壳煅烧成生石灰,并将生石灰制成石灰乳;
①将海边大量的贝壳煅烧成生石灰,并将生石灰制成石灰乳;
②将石灰乳加入到海水沉淀池中经过滤得到Mg(OH)2沉淀;
③在Mg(OH)2沉淀中加入盐酸得到MgCI2溶液,再经蒸发结晶得到MgCl2·6H2O;
④将MgCl2·6H2O在一定条件下加热得到无水MgCl2;
⑤电解熔融的氯化镁可得到Mg。
⑴步骤①中涉及的化学方程式为 。
⑵步骤③中的蒸发利用风吹日晒完成,但在实验室中蒸发操作时需要的主要仪器有 、 、酒精灯、三脚架、泥三角、坩埚钳等。
⑶海水中的镁以Mg2+形式存在,设计步骤②③将Mg2+转化为Mg(OH)2又重新转化为Mg2+的目的是 。
⑷步骤④中的“一定条件”指的是 ,目的是 。
⑸上述流程中,在降低成本、减少污染方面做了一些工作,请写出其中一点:

⑹有同学认为:可以在步骤②后加热Mg(OH)2得到MgO,再电解熔融的MgO制金属镁,以简化实验步骤,体现实验的简约性原则。你是否同意该同学的观点 (填“同意”或“不同意”),理由为 。
有关FeSO4的转化关系如下图所示(无关物质已略去)。
已知:① X由两种化合物组成,将X通入品红溶液,溶液褪色;通入BaCl2溶液,
产生白色沉淀。
② Y是红棕色的化合物。
(1)气体X的成分是(填化学式)。
(2)反应I的反应类型属于(填序号)。
a.分解反应 b.复分解反应 c.置换反应 d.化合反应 e.氧化还原反应
(3)溶液2中金属阳离子的检验方法是。
(4)若经反应I得到16 g固体Y,产生的气体X恰好被0.4 L 1 mol/L NaOH溶液完全吸收,则反应IV中生成FeSO4的离子方程式是。
浓硫酸具有A-D所示的性质,以下过程主要表现了浓硫酸的那些性质?请将选项字母填在下列各小题的括号内:
A强酸性 B 吸水性 C 脱水性 D 强氧化性
(1)浓硫酸可以干燥氢气
(2)浓硫酸使木条变黑
(3)热的浓硫酸与铜片反应
(1)80℃时,将0.40 mol的N2O4气体充入2L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4 (g)  2NO2 (g)△H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
2NO2 (g)△H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
| 时间(s) n(mol) |
0 |
20 |
40 |
60 |
80 |
110 |
| n(N2O4) |
0.40 |
a |
0.20 |
c |
d |
e |
| n(NO2) |
0.00 |
0.24 |
b |
0.52 |
0.60 |
0.60 |
①上表中c =___________;e =_____________
②计算20s—40s内用NO2表示的平均反应速率为mol/(L·s)
③计算在80℃时该反应的平衡常数K=;
(2)若(1)中反应进行至110s后,保持温度和体积不变,向容器中再加入0.2mol N2O4,此时,平衡朝_______方向移动;建立新平衡后,N2O4的转化率_______75%(填“>、<或=”);
(3)若(1)中反应进行至110s后,保持温度和体积不变,向容器中再加入0.2mol N2O4和0.1mol NO2时,v正________ v逆(填“>、<或=”)
请按要求回答下列问题:
(1)新出土的青铜器若保存不善,在潮湿的环境中容易生成铜绿,该腐蚀过程中的负极反应式为:_________________________。
(2)惰性电极电解饱和Na2S溶液时,在阳极附近没有看到预期的浑浊现象,探究发现,其生成了Na2Sx,则阳极反应式为:_____________________。当阳极产生1mol Sx2-时,阴极产生的气体在标准状况下的体积为_________L。(用含x的代数式表示)
(3)合成氨工业中,天然气能代替煤用于生产原料气——H2,且反应类似。请写出天然气转化为H2的两步反应方程式:______________________________________,
___________________________________________。
(4)已知:
| 酸 |
电离常数(Ka) |
酸 |
电离常数(Ka) |
| CH3COOH |
1.8×10-5 |
HCN |
5×10-10 |
| H2CO3 |
Ka1= 4.2×10-7 |
HClO |
3×10-8 |
| Ka2= 5.6×10-11 |
①上述四种酸中,酸性最强的是;
②25℃时,0.01 mol/L NaCN溶液的pH________7;
③在浓度均为0.01 mol/L的CH3COONa、NaClO、Na2CO3的混合溶液中,逐滴加入0.01 mol/L HCl,则体系中酸根离子反应的先后顺序为;
④25℃时,向20mL 0.1 mol/L CH3COOH溶液中逐滴滴加0.1mol/L NaOH溶液,体系中各种量随着NaOH溶液的加入而变化的图像正确的是_____________。

AB

C D
“84”消毒液可用来消毒,已知某品牌“84”消毒液的有效成分为NaClO,另外还有较大量的Na2CO3、NaCl,为探究该消毒液的性质,某同学做了如下实验:取少量消毒液并向其中通入过量的CO2,再滴入品红,发现品红很快褪色。
(1)写出向溶液中通入过量的CO2所发生的两个离子方程式:
。(2)使品红很快褪色的物质是 。
(3)以该消毒液为主要来源可以制备较纯净的少量Cl2,具体操作分两个主要步骤:先向消毒液中加入过量的A试剂,静置后取上层清液,再加入了硫酸。(提醒:最后发生的反应为:NaCl + NaClO + H2SO4 = Cl2↑+ Na2SO4 +H2O)
① A试剂的化学式为_____________,其作用是 。
② 若生成标准标况下5.6 L Cl2,则转移电子的物质的量为____________。