反应aA(g)+bB(g) cC(g)(
cC(g)(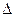 H<0)在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如下图所示:
H<0)在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如下图所示: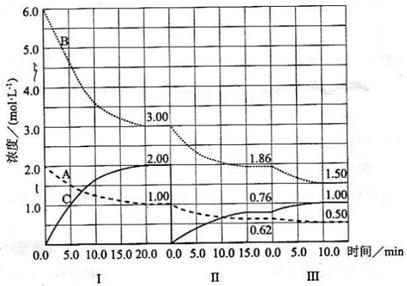
回答问题 :
:
(1)反应的化学方程式中,a:b:c为 ;
(2)B的平衡转化率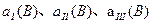 中最小的是 ,其值是 ;
中最小的是 ,其值是 ;
(3)由第一次平衡到第二次平衡,平衡移动的方向是 ,采取的措施是 ;
(4)比较第II阶段反应温度(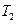 )和第III阶段反应速度(
)和第III阶段反应速度(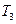 )的高低:
)的高低: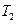
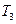 填“>、=、<”判断的理由是 。
填“>、=、<”判断的理由是 。
(1)在标准状况下,测得1.32 g某气体的体积为0.672 L。则此气体的摩尔质量为。
(2)等质量CO、CO2两种气体的的摩尔质量之比为;同温同压下的体积比为;其中氧元素的原子个数比为。
(3)常用食醋除去水壶中的水垢,以氢氧化镁为例,表明反应原理(用离子方程式表示)。
3 对甲苯丙烯酸甲酯(E)是一种用于合成抗血栓药的中间体,其合成路线如下:
对甲苯丙烯酸甲酯(E)是一种用于合成抗血栓药的中间体,其合成路线如下:
已知:HCHO+CH3CHO CH2=CHCHO+H2O。
CH2=CHCHO+H2O。
(1)遇FeCl3溶液显紫色的A的同分异构体有_______种。B中含氧官能团的名称为_____________。
(2)1molB最多能跟______molH2发生加成反应。
(3)试剂C可选用下列中的_____________。
a、溴水 b、银氨溶液 c、酸性KMnO4溶液 d、新制Cu(OH)2悬浊液
(4) 是E一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为__________________________________。
是E一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为__________________________________。
(5)E在一定条件下可以生成高聚物F,F的结构简式为_____________________________。
已知2A2(g)+B2(g)  2C3(g);△H=-Q1 kJ/mol(Q1>0), 在一个有催化剂的固定容积的容器中加入2 molA2和1 molB2,在500℃时充分反应,达平衡后C3的浓度为w mol·L-1,放出热量为Q2 kJ。
2C3(g);△H=-Q1 kJ/mol(Q1>0), 在一个有催化剂的固定容积的容器中加入2 molA2和1 molB2,在500℃时充分反应,达平衡后C3的浓度为w mol·L-1,放出热量为Q2 kJ。
(1)达到平衡时, A2的转化率为________。
(2)达到平衡后,若向原容器中通入少量的氩气,A2的转化率将_____(填“增大“、“减小”或“不变”)
(3)若在原来的容器中,只加入2mol C3,500℃时充分反应达平衡后,吸收热量Q3kJ,C3浓度(填>、=、<)w mol·L-1,Q1、Q2、Q3之间满足何种关系
(4)能说明该反应已经达到平衡状态的是。
a.v(C3)="2" v (B2); b.容器内压强保持不变
c.2v逆(A2)=v正(B2) d.容器内的密度保持不变
(5)改变某一条件,得到如图的变化规律
(图中T表示温度,n表示物质的量),可得出的结论正确的是;
a.反应速率c>b>a
b.达到平衡时A2的转化率大小为:b>a>c
c.T2>T1
d.b点A2和B2的物质的量之比为2:1
(6)若将上述容器改为恒压容器(反应前体积相同),起始时加入2 molA2和l molB2,500℃时充分反应达平衡后,放出热量Q4 kJ,则Q2Q4(填“>”、“<”或“=”)。
(7)下列措施可以同时提高反应速率和B2的转化率是(填选项序号)。
a.选择适当的催化剂b.增大压强
c.及时分离生成的C3d.升高温度
(12分)N2(g)+3H2(g)  2NH3(g)反应过程的能量变化如下图所示。
2NH3(g)反应过程的能量变化如下图所示。
已知生成1 mol NH3(g)的ΔH=-46 kJ·mol-1。请回答下列问题:
(1)图中A、C分别表示、;若该反应使用催化剂,会使图中B点升高还是降低?。
(2)图中ΔH=kJ·mol-1。
(3)已知恒容时,该体系中各物质浓度随时间变化的曲线如图所示。
①在0.5 L容器中发生反应,前20 min内,v(NH3)=________,放出的热量为________。
②45 min时采取的措施是_______________________。
③比较I、II、III时段的化学平衡常数(分别用K1、K2、K3表示)大小________。
(6分)在标准状况下,由CO和CO2组成的混合气体6.72 L,质量为12 g。此混合物中CO和CO2物质的量比是________,CO的体积分数是________,CO的质量分数是________,C和O原子个数比是________,混合气体的平均相对分子质量是________,对氢气的相对密度是________。