现有铁和铜组成的合金共a mol,其中铜的物质的量分数为x。将此合金研成粉末状后全部投入含b mol硝酸的稀溶液中,微热使其充分反应,硝酸的还原产物只有NO。
(1)用粒子符号填写下列空白(列举出全部可能出现的情况):
| 组序 成 分 |
① |
② |
③ |
④ |
⑤ |
⑥ |
| 残留固体成分 |
|
|
|
|
|
[ |
| 溶液中金属离子 |
|
|
|
|
|
|
(2)当溶液中金属离子只有Fe2+、Cu2+时,则b的取值范围为(用a、x表示)
(3)当x=0.5时,溶液中Fe3+和 Fe2+的物质的量相等,在标准状况下共生成672毫升NO气体,求a和b的值。
(10分)(1)维生素A的结构简式如下:
1 mol维生素A最多可与______mol H2发生加成反应。维生素A________(填“属于”或“不属于”)芳香化合物。
(2)在有机反应中,反应物相同而条件不同,可得到不同的主产物,下式中R代表烃基,副产物均已略去。
(Ⅰ)
(请注意H和Br加成的位置)
(Ⅱ)
请写出实现下列转变的各步反应的化学方程式,写明反应条件。
①由CH3CH2CH2CH2Br分两步转变为CH3CH2CHBrCH3:_________________________________;
②由(CH3)2CHCH===CH2分两步转变为(CH3)2CHCH2CH2OH:______________________________。
(10分)人们对苯及芳香烃的认识有一个不断深化的过程。
(1)由于苯的含碳量与乙炔相同,人们认为它是一种不饱和烃,写出分子式为 C6H6 的一种含两个叁键且无支链链烃的结构简式 。
(2)已知分子式为 C6H6 的结构有多种,其中的两种为
①这两种结构的区别表现在:
定性方面(即化学性质方面):Ⅱ能_______(选填a、b、c、d,多选扣分)而Ⅰ不能
a、被酸性高锰酸钾溶液氧化b、能与溴水发生加成反应,
c、能与溴发生取代反应d、能与氢气发生加成反应
定量方面(即消耗反应物的量的方面):1 mol C6H6 与H2加成时:
Ⅰ需______mol,而Ⅱ 需 _______mol。
②今发现C6H6还可能有另一种如右图立体结构:该结构的二氯代物有_______种。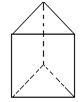
(8分)(1)下面列出了几组物质,请将物质的合适组号填写在空格上。
同位素 同素异形体 同分异构体 同一种物质 。
①金刚石与“足球烯”C60; ②D与T;
(2)写出下列反应方程式并注明反应类型
① ②
CH2=CH2 → CH3CH2OH → CH3COOCH2CH3
①
② 反应类型
(14分)金刚烷是一种重要的化工原料,工业上可通过下列途径制备:
请回答下列问题:
(1)环戊二烯分子中最多有______个原子共平面。
(2)金刚烷的分子式为__________。
(3)下面是以环戊烷为原料制备环戊二烯的合成路线:
其中,反应②的反应试剂和反应条件是___________,反应③的反应类型是____________,反应④的化学方程式为 。
(4)已知烯烃能发生如下反应: 。
。
请写出下列反应产物的结构简式: ____________________________。
____________________________。
(5)A是二聚环戊二烯的同分异构体,能使溴的四氯化碳溶液褪色,A经酸性高锰酸钾溶液加热氧化可以得到对苯二甲酸( )[提示:苯环上的烷基(—CH3,—CH2R,—CHR2)或烯基侧链经酸性高锰酸钾溶液氧化得羧基(—COOH)],写出A所有可能的结构简式(不考虑立体异构):_____________。
)[提示:苯环上的烷基(—CH3,—CH2R,—CHR2)或烯基侧链经酸性高锰酸钾溶液氧化得羧基(—COOH)],写出A所有可能的结构简式(不考虑立体异构):_____________。
现有五种有机物,请回答下列问题:
A.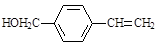 |
B.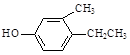 |
C. |
D. |
E.
F.
(1)A物质中含有的官能团名称为 、 。
(2)B的分子式为 。
(3)D的一氯代物最多有 种。
(4)上述化合物中互为同分异构体的是 ;互为同系物的是 。(填字母)