下列各组热化学方程式中,化学反应的ΔH前者大于后者的是( )
①C(s)+O2(g)===CO2(g) ΔH1
C(s)+O2(g)===CO(g) ΔH2
②S(s)+O2(g)===SO2(g) ΔH3;
S(g)+O2(g)===SO2(g) ΔH4
③H2(g)+O2(g)===H2O(l) ΔH5
2H2(g)+O2(g)===2H2O(l) ΔH6
④CaCO3(s)===CaO(s)+CO2(g) ΔH7
CaO(s)+H2O(l)===Ca(OH)2(s) ΔH8
| A.① | B.④ |
| C.②③④ | D.①②③ |
下列说法不正确的是
| A.乙醇和二甲醚互为同分异构体,利用红外光谱法或核磁共振氢谱法均可鉴别两者 |
| B.乙酸乙醋在碱性条件下水解,属于皂化反应 |
| C.使用含有氯化钠的融雪剂会加快桥梁的腐蚀 |
| D.道尔顿首次提出原子学说、汤姆生发现电子、卢瑟福确定原子核的存在,都为原子结构理论的发展作出了巨大贡献 |
某废水中可能存在的离子如下:Na+、Ag+、Ba2+、Al3+、AlO2一、CO32-、S2一、SO32-、SO42-
现取该溶液进行有关实验,实验过程及现象如下:
下列说法正确的是
| A.根据实验①中的现象可推出,气体A一定是纯净物,淡黄色沉淀一定是AgBr |
| B.根据实验②中的现象可推出,气体B是CO2,沉淀B是Al(OH)3,原溶液中一定含有Al3+ |
| C.根据实验③中的现象可推出,气体C是NH3,沉淀C一定有BaCO3,可能有BaSO4 |
| D.原溶液中肯定含有Na+、AlO2-、S2-,不能确定是否含有SO32-、SO42- |
下列图示与对应的叙述相符的是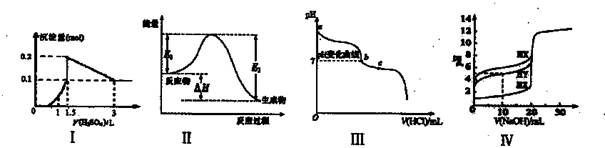
| A.图I表示向1L浓度均为0.1 mol/L的Ba(OH)2、NaAlO2混合液中逐滴加入0.1 mol/L稀H2SO4溶液,产生沉淀量的变化 |
| B.图Ⅱ中逆反应的热效应△H=E1- E2 <0,所以逆反应为放热反应 |
| C.图Ⅲ表示向20 mL 0.1 mol/L Na2CO3溶液中逐滴加入0.1 mol/L HCl溶液,溶液pH的变化,c点溶液中:c(HCO3一)+2c(CO32一)+c(C1-)>c(Na+) |
| D.用0.1 mol/L NaOH溶液分别滴定浓度相同的三种一元酸,由图Ⅳ曲线可确定HX的酸性最强 |
一种新型污水处理装置如图所示。该装置可利用一种微生物将有机废水的化学能直接转化为电能。下列说法中不正确的是
| A.电池工作时H+从M极区移向N极区 |
| B.N极为正极,发生还原反应 |
| C.M极的电极反应式为C6H12 O6 +6H2O-24e-=6CO2↑+24 H+ |
| D.当N极消耗5.6 L(标况下)气体时,则有2 NA个H+通过离子交换膜 |
下列说法正确的是
A.按系统命名法,有机物 的名称为3,7一二.甲基-4-乙基辛烷 的名称为3,7一二.甲基-4-乙基辛烷 |
B.高聚物脲醛树脂( )的合成单体之一是 )的合成单体之一是 |
| C.1 mol葡萄糖能水解生成2 rnol CH3CH2OH和2 mol CO2 |
| D.在酸性条件下,CH3CO18OC2 H5的水解产物是CH3CO18OH和C2H5OH |