(8分)废旧印刷电路板经粉碎分离能得到非金属粉末和金属粉末,回收利用可实现资源再生,减少污染。
⑴下列处理印刷电路板非金属粉末的方法中,不符合环境保护理念的是 (填字母)。
| A.热裂解形成燃油 | B.露天焚烧 | C.作为有机复合建筑材料的原料 | D.直接填埋 |
已知aAn+、bB(n+1)+、cCn-、dD(n+1)─具有相同的核外电子排布,则a、b、c、d由大到小的顺序是____________,这四种离子的半径由大到小的顺序是。
A.原子数相同、电子总数相同的分子,互称为等电子体。
Ⅰ.已知A、B、C、D和E五种分子所含原子的数目依次为1、2、3、6和6,且都含有18个电子,又知B、C和D是由两种元素的原子组成,且D分子中两种原子个数比为1 :2。
请回答:
(1)组成A分子的原子的元素符号是;已知E是有毒的有机物,E的熔、沸点比CH4的熔、沸点高,其主要原因是____________________________________。
(2)C的立体结构呈____ 形,该分子属于分子(填“极性”或“非极性”);
(3)火箭中可充入四氧化二氮和D作为燃料反应生成氮气和水,该反应的化学方程式为_________________________。(不需要写反应条件)
Ⅱ.CO与N2互为等电子体。
(4)CO的总键能大于N2的总键能,但CO比N2容易参加化学反应。
根据下表数据,说明CO比N2活泼的原因是____________________________________。
| A-B |
A=B |
A≡B |
||
| CO |
键能(kJ/mol) |
357.7 |
798.9 |
1071.9 |
| 键能差值kJ/mol) |
441.2 273 |
|||
| N2 |
键能(kJ/mol) |
154.8 |
418.4 |
941.7 |
| 键能差值kJ/mol) |
263.6 523.3 |
(5)它们的分子中都包含___________个σ键,______________个π键。
(6)Fe、Co、Ni等金属能与CO反应的原因与这些金属原子的电子层结构有关。
Ni原子的价电子排布式为_____。Fe(CO)5常温下呈液态,熔点为
-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)5晶体属于____(填晶体类型);Fe(CO)5是配合物,配体是__________。
B.茶中含有多种有益于人体健康的成分,据测定茶叶中含有450种以上的有机成分与15种以上的元素。某化学研究小组欲探究茶叶中钙元素的含量,设计了探究实验方案如下:(已知茶叶中的铝、铁元素对钙离子的测定有影响)
步骤1:称取500g干燥的茶叶,置于通风橱中,充分灼烧使茶叶灰化,再用研钵磨细后移入烧杯中,然后将200mL 1 mol·L-1盐酸加入灰中搅拌、过滤、洗涤。
步骤2:向步骤1所得滤液中逐滴加入稀氢氧化钠溶液,调节溶液的pH至6~7左右,使铝、铁元素以氢氧化物的形式完全沉淀,再加热煮沸30 min,加入7.95g无水碳酸钠,充分搅拌,待沉淀完全后,过滤,洗涤,过滤后得到滤液和沉淀。
步骤3:将步骤2所得的滤液稀释至500 mL,取其中的20.00 mL溶液以甲基橙作指示剂,用0.100mol·L-1的HCl标准溶液滴定,终点时消耗盐酸的体积为20.00mL,计算结果。
请回答下列问题:
步骤 1中,使茶叶灰化时需要用到三角架、泥三角、酒精喷灯、___、____等仪器。
步骤2中,改用试剂_______(写试剂名称)来调节pH将更为方便;判断沉淀已经洗净的方法是。
步骤3中,滴定过程中,眼睛应注视____________________,被滴定的20 mL滤液中含CO32-的物质的量为 __mol,试计算原500g茶叶中钙离子的质量分数为_______,计算过程如下:
设反应①Fe(s)+CO2(g)  FeO(s)+CO(g)的平衡常数为K1。
FeO(s)+CO(g)的平衡常数为K1。
反应②Fe(s)+H2O(g)  FeO(s)+H2(g)的平衡常数为K2,在不同温度下,K1、K2的值如下:
FeO(s)+H2(g)的平衡常数为K2,在不同温度下,K1、K2的值如下:
| T(K) |
K1 |
K2 |
| 973 |
1.47 |
2.36 |
| 1173 |
2.15 |
1.67 |
(1)平衡常数K1的表达式为________________ 。
(2)现有反应③ CO2(g) +H2(g)  CO(g) +H2O(g);△H>0,这是一个(填“吸”或“放”)热反应,要使反应③在一定条件下建立的平衡向右移动,可采取的措施的有。
CO(g) +H2O(g);△H>0,这是一个(填“吸”或“放”)热反应,要使反应③在一定条件下建立的平衡向右移动,可采取的措施的有。
A.缩小反应容器容积 B.扩大反应容器容积 C.降低温度
D.升高温度 E.使用合适的催化剂 F.设法减少CO的量
(3)若反应Fe(s)+CO2(g)  FeO(s)+CO(g)在温度T1下进行;Fe(s)+H2O(g)
FeO(s)+CO(g)在温度T1下进行;Fe(s)+H2O(g)  FeO(s)+H2(g)在温度T2下进行,已知T1>T2,且c(CO2)>c(CO)(其他条件均相同),则两者的反应速率(填序号)。
FeO(s)+H2(g)在温度T2下进行,已知T1>T2,且c(CO2)>c(CO)(其他条件均相同),则两者的反应速率(填序号)。
A.前者大 B.后者大 C.一样大 D.无法判断
(4)以下图像:(图中v为速率,φ为生成物的百分含量,T为温度)
其中符合反应①的是 _________(填图像序号,下同),符合反应②的是 ___。
(12分) 已知:CH2=CH—CH=CH2和CH3—CH=CH2分别可以写成: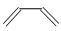 和
和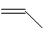 ;
;
“双烯合成反应”又称为“Diels-Alder反应”,如: 。
。
请回答下列问题:
(1)现有反应: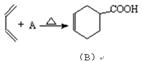 ,则物质A的结构式为:________________ ;
,则物质A的结构式为:________________ ;
在浓磷酸作用下,B与乙醇共热生成酯的化学方程式为:_________________________________________________。
(2)在反应: 中,D物质可发生反应生成一种生活中常用高分子,其化学方程式为:_____________;将物质E与过量的H2发生加成反应,其生成物的化学式为_________。
中,D物质可发生反应生成一种生活中常用高分子,其化学方程式为:_____________;将物质E与过量的H2发生加成反应,其生成物的化学式为_________。
(3) 和
和 都是无色液体,下列物质中可以用来鉴别这两种物质的是(填序号):①银氨溶液、②淀粉溶液、③溴水、④酸性KMnO4溶液;
都是无色液体,下列物质中可以用来鉴别这两种物质的是(填序号):①银氨溶液、②淀粉溶液、③溴水、④酸性KMnO4溶液;
物质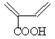 与物质
与物质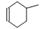 发生“Diels-Alder反应”的生成物为:___。
发生“Diels-Alder反应”的生成物为:___。
(4)从现代化学观点看,“Diels-Alder反应”的优点是:__________________________。
(10分)温家宝总理多次指出要大力抓好节能降耗、保护环境。请你分析并回答下列问题:
(1)“绿色化学”的最大特点在于它是在始端就采用预防实际污染的科学手段,因而过程和终端均为零排放和零污染,具有“原子经济性”。下列化学反应不符合“绿色化学”思想的是____________________。
A.制备环氧乙烷: |
B.制备硫酸铜Cu+2H2SO4 CuSO4+SO2↑+2H2O CuSO4+SO2↑+2H2O |
C.制备甲醇: 2CH4+O2 2CH3OH 2CH3OH |
| D.制备硝酸铜:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O |
(2)冶金废水中含有[Au(CN)2]-,其电离出的CN-有毒,当与H+结合生成HCN时,其毒性更强。工业上处理这种废水是在碱性条件下,用NaClO将CN-氧化为CO32-和一种无毒气体,该反应的方程式为_____________________________,在酸性条件下,ClO-也能将CN-氧化,但实际处理时却不在酸性条件下进行的主要原因是____________________________________________________________。
(3)工业上目前使用两种方法制取乙醛——“乙炔水化法”和“乙烯氧化法”。下面两表提供生产过程中原料、反应条件、原料平衡转化率和产量等的有关信息:
| 乙炔水化法 |
乙烯氧化法 |
|
| 原料 |
乙炔、水 |
乙烯、空气 |
| 反应条件 |
HgSO4、100~125℃ |
PdCl2-CuCl2、100~125℃ |
| 平衡转化率 |
乙炔平衡转化率90%左右 |
乙烯平衡转化率80%左右 |
| 日产量 |
2.5吨(某设备条件下) |
3.6吨(相同设备条件下) |
表一:原料、反应条件、平衡转化率、日产量
表二:原料来源生产工艺
| 原料生产工艺过程 |
|
| 乙炔 |
  |
| 乙烯 |
来源于石油裂解气 |
从两表中分析,现代工业上“乙烯氧化法”将逐步取代“乙炔水化法”的可能原因。
①从产率和产量角度分析。
②从环境保护和能耗角度分析。