某研究性学习小组,用下列仪器、药品验证足量合金(由Cu、Fe、Zn三种物质组成)和适量浓硝酸反应产生的气体中含NO(N2和O2的用量可自由控制,气体液化温度:
NO2:21℃,NO:-152℃)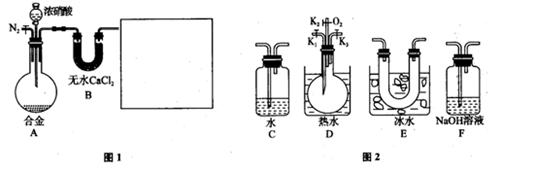
(1)在图2中选择恰当的仪器将图1补充完整,所选择仪器的连接顺序(按左→右连接,填各仪器编号)为_________(2分).
(2)反应前先通入N2目的是_______________________________________(2分).
(3)确认气体中含NO的现象是______________________ _________________(2分).
_________________(2分).
(4)本题中,浓硝酸(含溶质a mol)完全反应,还原产物只有NO和NO2,被还原硝酸的物质的量n的取值范围为_________________________________________(3分).
在常温、常压下,用铂作电极电解CuSO4溶液。通电一段时间,切断电源,一个电极的质量增加了0.127 g,另一电极的气体产物的质量应是__________g,溶液的pH________(填“增大”“减少”或“不变”)。
用铂电极电解氢氧化钠溶液,测定两极逸出气体的体积,记录如下
| 时间/min气体体积/L |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
| 阴极生成的气体 |
6 |
12 |
20 |
29 |
39 |
49 |
59 |
69 |
| 阳极生成的气体 |
2 |
4 |
7 |
11 |
17 |
23 |
28 |
34 |
(1)完成有关的电极反应式:阴极__________;阳极____________;
(2)完成电解的总化学方程式_______________________________;
(3)开始电解阶段两极产生气体的体积比不符合理论比值的原因是______________________;
(4)自第__________分钟起阴极与阳极产生气体的体积比约为理论的比值;
(5)该过程NaOH溶液的pH如何变化__________________________________。
试计算下列溶液的pH(均在25 ℃时):
(1)0.1 mol·L-1 NaOH溶液与0.1 mol·L-1 Ba(OH)2溶液等体积相混后溶液的pH为_____。
(2)将0.1 mol·L-1盐酸与0.6 mol·L-1Ba(OH)2溶液等体积相混后溶液的pH为________。
(3)将0.1 mol·L-1的稀H2SO4稀释1010倍后,溶液中c(H+)∶c( )=______________。
)=______________。
某学生在实验室测定溶液的pH时,先将pH试纸用蒸馏水润湿后再进行测定,其测定结果是否一定有误差?_____________,理由是_______________________________________。若用此方法分别测定c(H+)相等的H2SO4和H3PO4的pH,误差较大的是_____________,理由是_______________________________________。
如图4-6所示,甲是刚浸过Na2SO4溶液的滤纸,A、B两铜片通过导线连接电源两极,在铜片间的滤纸上滴一滴KMnO4溶液,通电一段时间后,发现A、B间紫红色圆点向A移动了一段距离,则与A相连的是电源的 极,可发现滤纸的 极边沿附近有 色出现。