已知某工业废水中含有大量CuSO4,少量的Ag+、Hg2+以及部分污泥,在实验室中通过下述过程可从该废水中回收硫酸铜晶体及其它物质。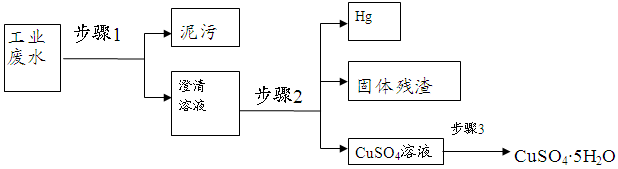
(1)步骤1的主要操作是 ,需用到的玻璃仪器除烧杯外有 。
(2)步骤2中需加入某种试剂后再将混合物分离,该试剂是(填化学式) ,生成固体残渣的的离子方程式 。
(3)步骤3中涉及的操作是:蒸发浓缩、 、过滤、烘干。
(4)步骤2应该在通风橱中进行,原因是 。
如图所示的装置,X、Y都是惰性电极。将电源接通后,向(甲)中滴入酚酞溶液,在Fe极附近显红色。试回答下列问题: 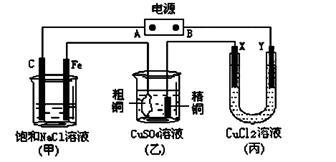
(1)在电源中,B电极为极(填电极名称,下同);丙装置中Y电极为极。
(2)在甲装置中,石墨(C)电极上发生反应(填“氧化”或“还原”);甲装置中总的化学方程式是:。
(3)丙装置在通电一段时间后,X电极上发生的电极反应式是。
(4)如果乙装置中精铜电极的质量增加了0.64g,请问甲装置中,铁电极上产生的气体在标准状况下为
L。
下图是红磷P(s)和Cl2反应生成 (图中的
(图中的 表示生成1mol产物的数据)。根据下图回答下列问题:
表示生成1mol产物的数据)。根据下图回答下列问题:
(1)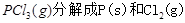 的热化学方程式为。
的热化学方程式为。
(2)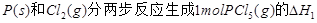 =KJ·mol-1
=KJ·mol-1
(3)研究表明,化学反应的能量变化(△H)与反应物和生成物的键能有关。键能可以简单地理解为断开1mol化学键时所需吸收的能量,表1所列是部分化学键的键能数据。
表1部分化学键的键能数据
| 化学键 |
P-P |
P-O |
O=O |
P=O |
| 键能/(kJ·mol-1) |
198 |
360 |
498 |
x |
已知1mol白磷(结构如下图所示,分子式为P4)完全燃烧生成P4O10(结构如下图)放出2982KJ热量,则表中:x=。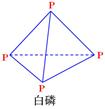 (P4O10)
(P4O10)
己知X、Y、Z、W、N、U、V是短周期的主族元素,原子序数依次增大。X与N同主族,且与W都能形成A2B、A2B2型化合物;Z、W的单质常温下均为无色气体;Y原子的L层电子数是K层电子数的2倍;U原子的最外层电子数是其电子层数的2倍,试回答下列问题:
(1)YW2的电子式;Z的氢化物结构式为;写出U元素在周期表中的位置。
(2)原子半径:UV(填>、<或=,下同);气态氢化物的水溶液的酸性:UV。
(3)写出UW2与V元素的单质在水溶液中反应的化学方程式是。
(4)由X、Z组成的一种化合物化学式为ZX5,其各原子均达到同周期稀有气体原子的稳定结构,该物质属于(填“离子”或“共价”)化合物。
(5)X、Y、Z、W四种元素(按顺序)可组成原子个数比为5:1:1:3的化合物,该化合物的稀溶液与足量氢氧化钠溶液在加热条件下反应的离子方程式为:。
(1)在下列物质中:①CO2②KOH ③He ④BaSO4⑤NaCl。其中只含有离子键的是(填序号,下同),既含有离子键又含有共价键的是,不含化学键的是。
(2)下列物质在所述变化中:①烧碱熔化 ②HCl气体溶于水 ③NH4Cl受热分解 ④干冰升华。其中化学键未被破坏的是(填序号,下同),仅发生共价键破坏的是,既发生离子键破坏,又发生共价键破坏的是。
某微粒的结构示意图为 , 试回答:
, 试回答:
(1)当x-y=10时,该粒子为(选填“原子”或“阳离子”、“阴离子”)。
(2)当y=8时,该粒子可能是(用化学式表示,任填3种)、、。
(3)请写出实验室制取y=7时元素对应单质的离子方程式:。