实验室用密度为1.18g/mL,质量分数为36.5%浓盐酸配制250mL0.1mol/L的盐酸溶液,若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响”):若移液后没有洗涤烧杯 ;若加蒸馏水时不慎超过了刻度线 ;若定容时俯视刻度线___________________;若量取浓盐酸仰视读数 。另外若定容时加蒸馏水不慎超过了刻度线应如何处理 。
氯化铁是常见的水处理剂,利用废铁屑可制备无水氯化铁,实验室制备装置和工业制备流程图如下: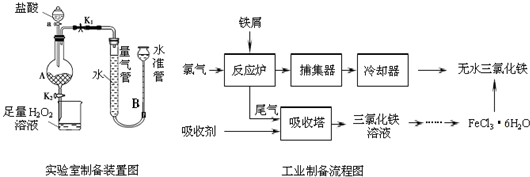
已知:(1)无水FeCl3的熔点为555K、沸点为588K.
(2)废铁屑中的杂质不与盐酸反应
(3)不同温度下六水合氯化铁在水中的溶解度如下:
| 温度/℃ |
0 |
20 |
80 |
100 |
| 溶解度(g/100g H2O) |
74.4 |
91.8 |
525.8 |
535.7 |
实验室制备操作步骤如下:
Ⅰ.打开弹簧夹K1,关闭弹簧夹K2,并打开活塞a,缓慢滴加盐酸.
Ⅱ.当…时,关闭弹簧夹K1,打开弹簧夹K2,当A中溶液完全进入烧杯后关闭活塞a.
Ⅲ.将烧杯中溶液经过一系列操作后得到FeCl3•6H2O晶体.
请回答:
(1)烧杯中足量的H2O2溶液的作用是______________________。
(2)为了测定废铁屑中铁的质量分数,操作Ⅱ中“…”的内容是______________________。
(3)从FeCl3溶液制得FeCl3•6H2O晶体的操作步骤是:加入______________后、_________________、蒸发浓缩、冷却结晶、过滤、洗涤、干燥。
(4)试写出吸收塔中反应的离子方程式:_____________________。
(5)捕集器温度超过673K时,存在相对分子质量为325的铁的氯化物,该物质的分子式为____________。
(6)FeCl3的质量分数通常可用碘量法测定:称取m g无水氯化铁样品,溶于稀盐酸,配制成100mL溶液;取出10.00mL,加入稍过量的KI溶液,充分反应后,滴入几滴淀粉溶液,并用c mol•L-1 Na2S2O3溶液滴定,消耗V mL(已知:I2+2S2O32-═2I-+S4O62-).
①滴定终点的现象是:_____________________。
②样品中氯化铁的质量分数________________。
(a)铁元素在人类生活中扮演着非常重要的角色,不仅仅是重要的建筑材料,也是人体必须的微量元素。每年钢铁的腐蚀带来巨大的经济损失。某校研究小组在实验室中模拟钢铁在自然环境下的腐蚀,设置如下装置,几天后观察结果:
请回答下列问题:
(1)请比较以上三个装置中右侧导管中红墨水的高度: > > 。请写出A装置中,钢铁锈蚀时正极反应的电极反应式 。
(2)钢铁的防腐有重大的意义,生活中常将金属制品放在干燥处或者涂上矿物油予以保护,现请你从电化学角度设计一种方法保护下图中钢铁以免被腐蚀,请将下图完成:
(b)下面是一种常见补铁药品说明书中的部分内容:该药品含Fe2+:33%~36%,不溶于水但能溶于人体中的胃酸,与Vc(维生素C)同服可增加本品吸收。某乙同学采用在酸性条件下用高锰酸钾标准溶液滴定的方法测定该药品是否合格,反应原理为:
5 Fe2++8H++MnO4-="5" Fe3++Mn2++4H2O
准确称量上述药品10.00g,将其全部溶于试剂1中,配制成1000mL溶液,取出20.00mL,用0.0200mol/L的KMnO4溶液滴定,用去KMnO4溶液12.00mL。
(3)该实验中的试剂1是 (填序号)。
A.蒸馏水B.稀盐酸C.稀硫酸D.稀硝酸
(4)请简述判断滴定终点的现象: 。
(5)请通过计算,说明该药品含铁量是否合格 (填“合格”或“不合格”)(Fe的摩尔质量为56g/mol)
聚合硫酸铁铝(PFAS)是一种新型高效水处理剂。利用硫铁矿烧渣(主要成分为Fe3O4、FeO、SiO2等)为铁源,粉煤灰(主要成分为Al2O3、Fe2O3、FeO等)为铝源,制备PFAS的工艺流程如下: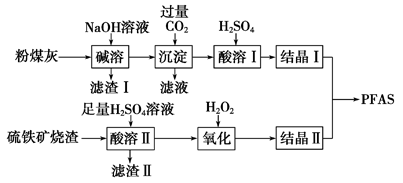
(1)“碱溶”时,Al2O3发生反应的化学方程式为______________________________。
(2)“酸溶Ⅱ”时,Fe3O4发生反应的离子方程式为____________________________。
(3)“滤渣Ⅰ”、“滤渣Ⅱ”在本流程中能加以利用的是_______________________。
(4)“氧化”时应控制温度不超过57 ℃,其原因是____________________________。
(5)“氧化”时若用MnO2代替H2O2,发生反应的离子方程式是____________________。
(6)酸度对絮凝效果和水质有显著影响。若产品PFAS中残留硫酸过多,使用时产生的不良后果是________________________。
某小组同学为探究H2O2、H2SO3、Br2氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)。
实验记录如下:
| 实验操作 |
实验现象 |
|
| Ⅰ |
打开活塞a,滴加氯水,关闭活塞a |
A中溶液变为红棕色 |
| Ⅱ |
吹入热空气 |
A中红棕色明显变浅;B中有气泡,产生大量白色沉淀,混合液颜色无明显变化 |
| Ⅲ |
停止吹入空气,打开活塞b,逐滴加入H2O2溶液 |
开始时颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色 |
请回答下列问题:
(1)A中反应的离子方程式是______________________________。
(2)实验操作Ⅱ吹入热空气的目的是________________________。
(3)装置C的作用是______________,C中盛放的药品是______________________。
(4)实验操作Ⅲ,混合液逐渐变成红棕色,其对应的离子方程式___________________。
(5)由上述实验得出的结论是______________________。
(6)实验反思:
①有同学认为实验操作Ⅱ吹入的热空气,会干扰(5)中结论的得出,你认为是否干扰,理由是__________________________。
②实验操作Ⅲ,开始时颜色无明显变化的原因是(写出一条即可):_____________________。
某兴趣小组拟制备K3[Fe(C2O4)3]·3H2O晶体
Ⅰ.查阅资料
K3[Fe(C2O4)3]·3H2O是翠绿色晶体,易溶于水,难溶于乙醇,具有光敏性,光照分解。
110℃失去结晶水,230℃时分解。K3[Fe(C2O4)3]·3H2O的摩尔质量是491g/moL
Ⅱ.制备产品
实验步骤如下:
① 取27.8gFeSO4·7H2O和K2C2O4反应生成草酸亚铁
② 将草酸亚铁(FeC2O4)和适量K2C2O4的混合溶液置于40℃的恒温水浴中,逐滴加入 6% H2O2,边加边搅拌,使Fe2+充分被氧化。反应体系中生成K3[Fe(C2O4)3]的同时还有部分Fe(OH)3沉淀
③ 向②所得浊液中加入1mol/LH2C2O4溶液,使溶液变为翠绿色
④ 加热浓缩,冷却结晶,过滤,洗涤,干燥,称量产品的质量为ag
请回答下列问题:
(1)第②步需要控制水浴40℃,温度不能太高的主要目的: ,若第④步冷却时间较长,需将溶液置于冷暗处,原因是: 。
(2)第②步中,为检验Fe2+是否已完全被氧化,可选用 。试剂(填字母)
| A.NaOH溶液 | B.K3Fe(CN)6溶液 | C.苯酚溶液 | D.KSCN溶液 |
(3)请写出第③步中加入H2C2O4溶液将Fe(OH)3沉淀反应生成K3[Fe(C2O4)3]的化学反应方程式: 。
(4)步骤④中的实验操作需要下列仪器中的 (填仪器的编号).
①酒精灯 ②燃烧匙 ③烧杯 ④广口瓶 ⑤研钵 ⑥玻璃棒
(5)有同学为提高产率,避免第④步加热浓缩过程中K3[Fe(C2O4)3]的少量分解,依据查阅的资料提出新的结晶方案:将步骤③得到的溶液中加入 ,过滤,洗涤,干燥,称量。