Ⅰ某化学过程的示意图如图所示。在装置工作过程中,甲池的总反应式为: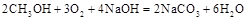 。
。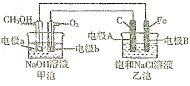
试回答下列问题:
(1)甲池溶液中的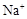 移向 (填“a”或“b”)电极,
移向 (填“a”或“b”)电极,
乙池溶液中的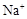 移向 (填“ A”或“B”)电极;
移向 (填“ A”或“B”)电极;
(2)电极a上发生的电极反应式为 ; (3)乙池中发生反应的离子方程式为 ;
(3)乙池中发生反应的离子方程式为 ;
(4)当电极A处得到0.71g产物时,甲池中理论上消耗
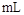 (标准状况下)。如何检验A处的产物 。
(标准状况下)。如何检验A处的产物 。
Ⅱ某研究性学习小组对铝热反应实验展开研究。现行高中化学教材对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”。查阅《化学手册》知,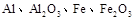 熔点、沸点数据如下:
熔点、沸点数据如下:
| 物质 |
Al |
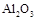 |
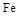 |
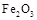 |
| 熔点/℃ |
660 |
2054 |
153 |
14 62 62 |
| 沸点/℃ |
2467 |
2980 |
2 750 750 |
- |
(1) 某同学推测,铝热反应所得到的熔融物应是铁铝合金。理由是:该反应放出的热量使铁熔化,铝的熔点比铁低,此时液态的铁和铝熔合形成铁铝合金。你认为他的解释是否合理 (填“合理”或“不合理”)
(2) 用一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所用试剂 ,反应的离子方程式为  。
。
(3) 实验室溶解该熔融物,下列 试剂中最适宜的试剂是
试剂中最适宜的试剂是
A.浓硫酸 B.稀硫酸 C.稀硝酸 D. 氢氧化钠溶液
图是等质量的Na2CO3、NaHCO3粉末分别与足量的盐酸发生反应时的情景,产生CO2气体的体积较多的试管中加入的固体试剂是________,当反应结束时,A、B两试管中消耗的盐酸的质量之比为__________。实验过程中我们还能感受到Na2CO3与盐酸反应时是放热反应,而NaHCO3与盐酸反应时表现为吸热。在A、B两试管中的此反应过程中,反应体系的能量变化的总趋势分别对应于A-____,B-____。(填写a或b)
(a)(b)
拆开1molH-H键、1molN-H键、1mol氮氮三键分别需要能量436kJ、391kJ、946kJ,
则(1)1molN2生成NH3的反应热是,
(2)1molH2生成NH3的反应热是。
共价键、离子键和分子间作用力都是微粒之间的作用力,有下列晶体: A.白磷、 B.金刚石、 C.氯化钠、 D.冰、 E.氢氧化钠、 F.二氧化硅。请用字母(A、B、…)回答以下问题:(共6分)
以上物质中,(1)熔点最低的是________;(2)属于分子晶体的物质是______________;
(3)含有离子键的物质是____________;(4)含有两种化学键的物质是_________。
在下列①NH3、②NH4Cl、③金刚石、④KBr、⑤甲烷、⑥CO2、⑦Ar七种物质中,请用编号填空:其中只含有离子键的是,只含有共价键且为直线型分子的是,空间构型为正四面体结构的分子是,熔点最高的是,不存在化学键的物质是。
下图表示4个碳原子相互结合的方式。小球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢结合。
(1)图中属于烷烃的是(填字母)。
(2)在上图的有机化合物中,碳原子与碳原子之间不仅可以形成共价单键,还可以形成和;不仅可以形成,还可以形成碳环。
(3)上图中互为同分异构体的是:A与;B与;D与。(填字母)