丙烷燃烧可以通过以下两种途径:
途径I:C3H8(g) + 5O2(g) ="=" 3CO2(g) +4H2O(l) ΔH=-a kJ·mol-1
途径II:C3H8(g) ==C3H6(g)+ H2(g) ΔH=+b kJ·mol-1
H2(g) ΔH=+b kJ·mol-1
2C3H6(g)+ 9O2(g) ="=" 6CO2(g) +6H2O(l) ΔH=-c kJ·mol-1
2H2(g)+O2 (g) == 2H2O(l) ΔH=-d kJ·mol-1(abcd均为正值)
请回答下列问题:
(1)判断等量的丙烷通过两种途径放出的热量,途径I放出的热量 ______(填“大于”、“等于”或“小于”)途径II放出的热量
(2)由于C3H8(g) ==C3H6(g)+ H2(g) 的反应中,反应物具有的总能量______(填“大于”、“等于”或“小于”)生成物具有的总能量,那么在化学反应时。反应物就需要______(填“放出”、或“吸收”)能量才能转化为生成物,因此其反应条件是______________
(3)b 与a、c、d的数学关系式是______________
乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平。请回答下列问题。
(1)乙烯的电子式____________,结构简式___________。
(2)鉴别甲烷和乙烯的试剂是______(填序号)。
A.稀硫酸 B.溴的四氯化碳溶液 C.水 D.酸性高锰酸钾溶液
(3)下列物质中,可以通过乙烯加成反应得到的是______(填序号)。
A.CH3CH3 B.CH3CHCl2C.CH3CH2OH D.CH3CH2Br
下表列出了①~⑨九种元素在周期表中的位置:
| ⅠA |
ⅧA |
|||||||
| 1 |
① |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
| 2 |
② |
③ |
④ |
⑧ |
||||
| 3 |
⑤ |
⑥ |
⑦ |
⑨ |
请按要求回答下列问题。
(1)元素④在周期表中所处位置____________,从元素原子得失电子的角度看,元素④具有____________性(填“氧化性”、“还原性”);
(2)按气态氢化物的稳定性由弱到强的顺序排列,⑥④⑦的氢化物稳定性:___________________________________(写氢化物的化学式);
(3)元素⑦的原子结构示意图是____________;
(4)写出元素⑤形成的单质在氧气中燃烧的化学方程式______________________,这一反应是___________(填“吸热”、“放热”)反应;
(5)用电子式表示①与⑨反应得到的化合物的形成过程_________________________。
原电池是一种________________________装置。电子表所用的某种钮扣电池的电极材料为Zn和Ag2O,电解质溶液为KOH,其电极反应式为:
Zn+2OH--2e-=ZnO+H2O Ag2O+H2O+2e-=2Ag+2OH-
电池的负极是____________,正极发生的是____________反应(填反应类型),总反应式为___________________________________。
(1)在 H、
H、 H、
H、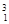 H、
H、 Mg、
Mg、 Mg和
Mg和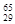 Cu中共有______种元素,______种原子。
Cu中共有______种元素,______种原子。
(2) 射线是由粒子组成的,粒子是一种没有核外电子的粒子,它带有2个单位正电荷,它的质量数等于4,由此推断粒子带有_________个中子。
有下列各组物质:
A.Al(OH)3与H3AlO3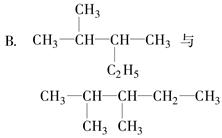
C.金刚石与石墨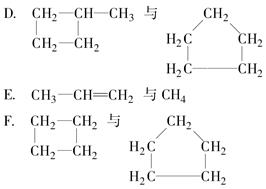
(1)互为同素异形体的是________。
(2)属于同系物的是________。
(3)互为同分异构体的是________。
(4)属于同一物质的是________。