⑴24 mL 0.05 mol·L-1的Na2SO3溶液恰好被20 mL 0.02 mol·L-1的K2R2O7溶液氧化,则元素R在还原产物中的化合价是________。
⑵将0.64 g Cu全部溶于一定量的浓硝酸中,测得生成气体0.009 mol(含NO、NO2和N2O4),共消耗硝酸0.032 mol。将生成的气体与空气混合,再通入NaOH溶液中,氮氧化物被完全吸收,产物只有NaNO3和H2O。计算空气中参加反应的O2在标准状况下的体积为________mL。
(1)卤素元素包括______、______、______ 、______(填元素符号),随核电荷数递增,它们的原子半径依次_______,单质的氧化性依次_______。
(2)在1-18号元素中(稀有气体元素除外),元素所形成的最稳定的气态氢化物是________;与水或酸反应最剧烈的单质是________;最高价氧化物的水化物中碱性最强的碱是__________;最高价氧化物的水化物中酸性最强的酸是__________。(填化学式)
五种短周期元素A、B、C、D、E,原子序数依次增大,其中A、B同周期,且A、B原子核外均有两个未成对电子;A、D同主族,B、E同主族,且C的最外层电子比E的最外层电子少5个。根据以上信息,完成下列各题。
(1)写出下列化学用语:A:B:C:D:E:
(2)A的最高价氧化物的熔点D的最高价氧化物的熔点(填“>”或“<”),原因是;B氢化物的沸点E氢化物的沸点(填“>”或“<”),原因是。
(3)选取上述五种元素,完成下列问题
①构成的原子晶体有;
②含有非极性键的离子化合物(用电子式表示)
③含有极性键的非极性分子(用电子式表示)
现有X、Y、Z、W四种短周期元素。
①X元素的单质在Y元素的单质中燃烧发出苍白色火焰,并生成气体A。
②Z元素的单质与A的水溶液反应又生成X元素的单质。
③Z元素的原子和Y元素的原子电子层数相同,且它们的最外层电子数之差的绝对值为奇数。
④W元素的原子核外有3个电子层,其最外层电子数等于电子层数。
请回答下列问题:
(1)X的元素符号为:_________;Z的元素名称是:。
(2)A的电子式是。
(3)Z的单质与A的溶液反应的离子方程式。
(4)W的氧化物溶于NaOH中的化学方程式。
第三主族的元素由于最外能层的p能级中有空轨道,故称为缺电子元素。
(1)已知气态氯化铝的化学式为Al2Cl6,写出Al2Cl6的结构式____________________;
(2)硼酸的结构式可表示为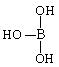 ,但硼酸溶于水后,1个硼酸分子与水作用,只能产生1个H+,请写出硼酸溶于水后溶液显酸性的离子方程式:(共4分)
,但硼酸溶于水后,1个硼酸分子与水作用,只能产生1个H+,请写出硼酸溶于水后溶液显酸性的离子方程式:(共4分)
不同元素的气态原子失去最外层一个电子所需要的能量(设其为E)如右图所示。试根据元素在周期表中的位置,分析图中吗线的变化特点,并回答下列问题。
(1)同主族内不同元素的E值变化的特点是:__________________________,各主族中E值的这种变化特点体现了元素性质的__________变化规律。
(2)同周期内,随原子序数增大,E值增大。但个别元素的E值出现反常现试预测下列关系式中正确的是______(填写编号,多选倒扣)
①E(砷)>E(硒)②E(砷)<E(硒)
③E(溴)>E(硒)④E(溴)<E(硒)
(3)估计1mol气态Ca原子失去最外层一个电子所需能量E值的范围:_____________<E<__________
(4)10号元素E值较大的原因是___________________