右表为元素周期表前四周期的一部分,下列有关B、W、X、Y、Z五种元素的叙述中,正确的是( )
A.常压下,五种元素的单质中 ,Z单质的沸点最高
,Z单质的沸点最高
B.W的氢化物比X的氢化物的稳定性高
C.Y、Z的阴离子电子层结构都与B原子的相同
D.Y元素比W元素的非金属性强
硒为第四周期VIA族元素,根据它在元素周期表中的位置推断,硒不可能具有的性质是()
| A.H2SeO4的酸性比H2SO4的酸性强 | B.其单质在通常状况下是固体 |
| C.硒元素有+4、+6、-2三种常见化合价 | D.SeO3的水化物为酸 |
关于元素周期表,下列叙述中不正确的是()
| A.周期表中的族分为:主族、副族、0族和VIII族 |
| B.周期表中的周期分为:短周期、长周期和不完全周期 |
| C.过渡元素全部是副族元素 |
| D.由短周期元素和长周期元素共同组成的族称为主族(除0族外) |
已知短周期元素的离子aX2+、bY+、cZ2-、dW- 都具有相同的电子层结构,则下列叙述正确的是()
| A.原子半径:X>Y>W>Z | B.离子半径:Z2- > W- > Y+ > X2+ |
| C.原子序数:d > c > b > a | D.原子的最外层电子数目:X>Y>W>Z |
2012年1月15日,我国广西省龙江河检测出重金属镉含量严重超标,重金属镉具有毒性,长期过量接触镉会引起慢性中毒,影响人体肾功能。镉元素有多种核素,下列关于95 48Cd和97 48Cd说法正确的是()
| A.95 48Cd和97 48Cd互为同素异形体 | B.95 48Cd和97 48Cd质量数相同 |
| C.95 48Cd和97 48Cd是同一种核素 | D.95 48Cd和97 48Cd互为同位素 |
把一块镁铝合金投入到1mol/L盐酸中,待合金完全溶解后,再往溶液里加入1mol/LNaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积的变化如图所示。下列说法中错误的是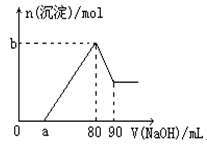
| A.盐酸的体积为80mL | B.a的取值范围为0<a<50 |
| C.n(Mg2+)<0.025mol | D.当a值为30时,b值为0.01 |