决定物质性质的重要因素是物质结构。请回答下列问题。
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如下表所示:
| 电离能/kJ·mol-1 |
I1 |
I2 |
I3 |
I4 |
| A |
578 |
1817 |
2745 |
11578 |
| B |
738 |
1451 |
7733 |
10540 |
A通常显 价,A的电负性 B的电负性(填“>”、“<”或“=”)。
(2)紫外光的光子所具有的能量约为399 kJ·mol-1。根据下表有关蛋白质分子中重要化学键的信息,说明人体长时间照射紫外光后皮肤易受伤害的原因: 。组成蛋白质的最简单的氨基酸中的碳原子杂化类型是 。
| 共价键 |
C-C |
C-N |
C-S |
| 键能/ kJ·mol-1 |
347 |
305 |
259 |
(3)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如下图所示),其中3种离子晶体的晶格能数据如下表: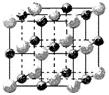
| 离子晶体 |
NaCl |
KCl |
CaO |
| 晶格能/kJ·mol-1 |
786 |
715 |
3401 |
则该 4种离子晶体(不包括NaCl)熔点从高到低的顺序是: 。
其中MgO晶体中一个Mg2+周围和它最邻近且等距离的Mg2+有 个。
(4)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是 。
(5)某配合物的分子结构如右图所示,其分子内不含有 (填序号)。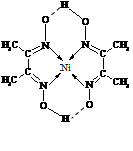
A.离子键 B.极性键 C.金属键
D.配位键 E.氢键 F.非极性键
以淀粉A为原料可以制得有茉莉花香味的H,现按以下方式进行合成该香料(方框中A、B、C、D、E、F均为有机物,同时方框中某些无机产物省略)
已知:RCH2Cl+NaOH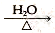 RCH2OH+NaCl
RCH2OH+NaCl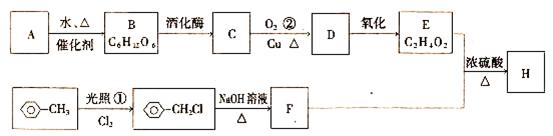
请回答下列问题:
(1)A的化学式为______,B的名称为______。
(2)写出①②的反应类型:①______,②______。
(3)C→D的化学方程式为______,
(4)F+E→H的化学方程式为______,
(5)写出C的两种同分异构体的结构简式______、______。
A、B、C、D、E、F六种短周期元素的原子序数依次增大,已知:①A原子半径最短;②B原子最外层电子数是次外层电子数的2倍;③C原子最外层电子数比次外层电子数多4个;④D原子的次外层电子数是最外层电子数的8倍;⑤E单质既能和盐酸反应又能和烧碱反应;⑥F与C同主族。回答下列问题:
(1)在六种元素中,形成物质种类最多的是______(填元素名称);
(2)写出C元素所有的氢化物的电子式______;
(3)用电子式表示D2F的形成过程______;
(4)A2C的沸点比A2F的沸点高的主要原因______;
(5)写出E与烧碱溶液反应的离子方程式______。
下列各组物质:

其中互为同位素的是_______;互为同素异形体的是_______;互为同系物的是_______;
互为同分异构体的是_______;属于同种物质的是_______。(用序号填空,下同)
(2)关于物质①K2O②CO2③NH4Cl ④C2H4⑤Na2O2⑥NaOH,请回答下列问题:仅含极性键和非极性键的化合物是_____;含有非极性键的离子化合物是_______。
(3)试计算烷烃中碳元素的质量分数的取值范围为_______。
已知X和Y均是元素周期表中同一主族元素的单质,W、V是化合物,它们有如下反应:(式中各物质的化学计量数及反应条件均已略去)X+W→Y+V
试写出符合题意且满足下列要求的化学方程式
① W是H2O:②V的水溶液是酸:
③W、V都是氧化物:④V是水:
A、B、C、D、E五种短周期元素,它们的原子序数依次增大。B原子的最外层电子数是其次外层电子数的2倍;A的一种原子中,质量数与质子数之差为零。D元素的原子最外层电子数为m,次外层电子数为n;E元素的原子L层电子数为m+n,M层电子数为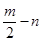 。请回答下列问题:
。请回答下列问题:
(1)D元素在周期表中的位置是_____________________;
(2)写出一个E和D形成的化合物与水反应的离子方程式_______________________;
(3)已知:甲 + H2O → 丙 + 丁。若甲是由N和Cl元素组成的化合物,其分子结构模型如右图所示,丙具有漂白性。则甲中Cl元素的化合价是 ,丁与H2O有相同的电子总数,则丁的化学式为。 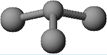
(4)与D同主族上下相邻的元素M、N,原子电子层数M>N>D,三种元素氢化物沸点由大到小的顺序是(填写化学式)。
(5)写出B与D在高温下完全反应后生成物的电子式___ __,结构式___