有机物A可作为合成降血脂药物安妥明( )和
)和
某聚碳酸酯工程塑料
( )的原料之一。
)的原料之一。
已知:
①如下有机物分子结构不稳定,会发生反应: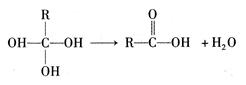
②某些醇或酚可以与碳酸酯反应生成聚碳酸酯,如:
相关的合成路线如下图所示:
(1)经质谱测定,有机物A的相对分子质量为58,燃烧2.9g有机物A,生成标准状况下3.36L CO2和2.7g H2O,A的核磁共振氢谱只出现一个吸收峰。则A的分子式是 。
(2)E→安妥明反应的化学方程式是 。
(3)C可能发生的反应类型是(填选项序号) 。
a. 取代反应 b. 加成反应 c. 消去反应 d. 还原反应
(4)F的结构简式是 。
(5)写出同时符合下列条件的E的同分异构体X的结构简式(只写1种即可)
。
①X能与饱和溴水发生取代反应
②X的苯环上有2个取代基,且苯环上的一溴取代物只有2种
③1mol X与足量NaHCO3溶液反应生成1mol CO2,与足量Na反应生成1mol H2
④X与NaOH水溶液发生取代反应所生成的官能团能被连续氧化为羧基
工业上用某矿渣(含有Cu2O、Al2O3、Fe2O3、SiO2)提取铜的操作流程如下:
已知:Cu2O+2H+=Cu+Cu2++H2O
(1)实验操作Ⅰ的名称为________;在空气中灼烧固体混合物D时,用到多种硅酸盐质的仪器,除玻璃棒、酒精灯、泥三角外,还有________(填仪器名称)。
(2)滤液A中铁元素的存在形式为________(填离子符号),生成该离子的离子方程式为_______________________________________________
________,检验滤液A中存在该离子的试剂为________(填试剂名称)。
(3)金属单质E与固体混合物F发生的某一反应可用于焊接钢轨,该反应的化学方程式为_____________________________________________________。
(4)常温下,等pH的NaAlO2和NaOH两份溶液中,由水电离出的c(OH-)前者为后者的108倍。则两种溶液的pH=________。
(5)①利用电解法进行粗铜精炼时,下列叙述正确的是________(填代号)。
a.电能全部转化为化学能
b.粗铜接电源正极,发生氧化反应
c.精铜作阴极,电解后电解液中Cu2+浓度减小
d.粗铜精炼时通过的电量与阴极析出铜的量无确定关系
②从浓硫酸、浓硝酸、蒸馏水中选用合适的试剂,测定粗铜样品中金属铜的质量分数,涉及的主要步骤:称取一定质量的样品→______________→过滤、洗涤、干燥→称量剩余固体铜的质量。(填缺少的操作步骤,不必描述操作过程的细节)
已知A~F六种常见物质中,B是空气的主要成分之一,其他均是常见的化合物,其中E是一种常见的溶剂,F是一种温室气体。它们之间的转化关系如图所示。下列说法中正确的是( )。
| A.化合物A是一种碱性氧化物 |
| B.图中①②③三个反应均为氧化还原反应 |
| C.化合物D是一种强碱 |
| D.化合物C的水溶液呈酸性 |
[有机化学基础]一种新型黏合剂E的结构简式为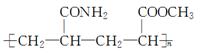 ,通过丙烯可制得E,其工业合成路线如图所示:
,通过丙烯可制得E,其工业合成路线如图所示: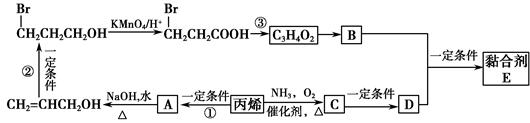
已知:2CH2=CHCH3+2NH3+3O2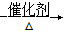 2CH2=CHCN+6H2O
2CH2=CHCN+6H2O
请回答下列问题:
(1)D的结构简式为______________。
(2)写出反应类型:反应①________;反应③________。
(3)反应②和③的目的是________________;反应③的条件是______________________________。
(4)写出2种具有酸性的B的同分异构体:________、________。
(5)写出B和D反应的化学方程式:________________________________
_________________________________________________________________。
[物质结构与性质]碳是形成化合物种类最多的元素。
(1)CH2=CH—C≡N是制备腈纶的原料,其分子中σ键和π键的个数之比为________(填最简整数比),写出该分子中所有碳原子的杂化方式:________________。
(2)乙醇(CH3CH2OH)和二甲醚(CH3OCH3)的分子式均为C2H6O,但CH3CH2OH的沸点高于CH3OCH3的沸点,其原因是_______________________________。
(3)某元素位于第四周期Ⅷ族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的价层电子排布式为________________。
(4)碳化硅的结构与金刚石类似,其硬度仅次于金刚石,具有较强的耐磨性能。如图所示为碳化硅的晶胞(其中 为碳原子,
为碳原子, 为硅原子)。每个碳原子周围与其距离最近的硅原子有________个。设晶胞边长为a cm,密度为b g·cm-3,则阿伏加德罗常数可表示为________(用含a、b的式子表示)。
为硅原子)。每个碳原子周围与其距离最近的硅原子有________个。设晶胞边长为a cm,密度为b g·cm-3,则阿伏加德罗常数可表示为________(用含a、b的式子表示)。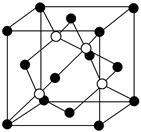
能源的开发利用与人类社会的可持续发展息息相关。
Ⅰ.已知:Fe2O3(s)+3C(s)=2Fe(s)+3CO(g)ΔH1=a kJ·mol-1
CO(g)+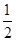 O2(g)=CO2(g) ΔH2=b kJ·mol-1
O2(g)=CO2(g) ΔH2=b kJ·mol-1
4Fe(s)+3O2(g)=2Fe2O3(s) ΔH3=c kJ·mol-1
则C的燃烧热ΔH=________ kJ·mol-1。
Ⅱ.(1)依据原电池的构成原理,下列化学反应在理论上可以设计成原电池的是________(填序号)。
A.C(s)+CO2(g)=2CO(g)
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)
C.2H2O(l)=2H2(g)+O2(g)
D.2CO(g)+O2(g)=2CO2(g)
若以熔融的K2CO3与CO2为反应的环境,依据所选反应设计成一个原电池,请写出该原电池的负极反应:______________________________________
_______________________________________________________________。
(2)某实验小组模拟工业合成氨反应N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ·mol-1,开始他们将N2和H2混合气体20 mol(体积比1∶1)充入5 L合成塔中,反应前压强为p0,反应过程中压强用p表示,反应过程中
2NH3(g) ΔH=-92.4 kJ·mol-1,开始他们将N2和H2混合气体20 mol(体积比1∶1)充入5 L合成塔中,反应前压强为p0,反应过程中压强用p表示,反应过程中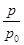 与时间t的关系如图所示。
与时间t的关系如图所示。
请回答下列问题: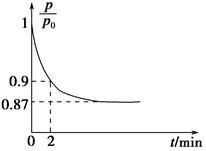
①反应达平衡的标志是(填字母代号)________。
A.压强保持不变
B.气体密度保持不变
C.NH3的生成速率是N2的生成速率的2倍
②0~2 min内,以c(N2)变化表示的平均反应速率为________。
③欲提高N2的转化率,可采取的措施有________。
A.向体系中按体积比1∶1再充入N2和H2
B.分离出NH3
C.升高温度
D.充入氦气使压强增大
E.加入一定量的N2
(3)25 ℃时,BaCO3和BaSO4的溶度积常数分别是8×10-9和1×10-10,某含有BaCO3沉淀的悬浊液中,c(CO32—)=0.2 mol·L-1,如果加入等体积的Na2SO4溶液,若要产生BaSO4沉淀,加入Na2SO4溶液的物质的量浓度最小是________ mol·L-1。