(8分)在一体积为1 L的容器中,通入一定量的N2 O4,在100℃时发生如下反应:
(1)在0-60s这段时间内,以N2O4表示的平均反应速率为 mol·L-1·s-1
(2)上述反应的平衡常数表达式为 ,升高温度K值 (填“增大"、“减小”或“不变”)
(3)反应进行到100s时,若有一项条件发生变化,变化的条件不可能是 (填选项序号)。
| A.降低温度 | B.通人氦气使其压强增大 | C.又往容器中充入N2O4 | D.使用催化剂 |
下表是三个不同短周期部分元素的原子半径及其主要化合价:
| 元素代号 |
W |
R |
X |
Y |
Z |
| 原子半径/nm |
0.037 |
0.157 |
0.066 |
0.070 |
0.077 |
| 主要化合价 |
+1 |
+1 |
-2 |
-3、+5 |
+2、+4 |
试回答下列问题:
(1)五种元素中原子半径最大的元素在周期表中位于。
(2)写出下列有关反应的化学方程式:
①Z的单质与Y元素的最高价氧化物对应的水化物反应:
;
②R2X2与ZX2反应:。
(3)X可与Z形成一种有恶臭味的气体,该气体与氧气发生反应的物质的量之比为1:2,且反应前后气体的总体积不变,试写出该气体分子(分子中各原子最外层均满足8e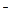 结构,且含有非极性键)的电子式:。
结构,且含有非极性键)的电子式:。
太湖、巢湖、滇池是我国重点治理的三大湖,三大湖受到严重的富营养化污染,藻类疯狂繁殖,破坏了生态平衡,影响了人民的健康,必须迅速进行治理。请回答:
(1)藻类的狂长,说明水中哪些元素超标?这些元素从哪里引入的?
(2)您认为引起藻类大量繁殖最主要的是哪一种元素?以什么形态出现?请你设计一个测定此元素的方法。
(3)水质污染程度的重要标志之一为BOD(生物化学耗氧量),它是指由于水中微生物的繁殖或呼吸作用,或水中有机物分解时所消耗的溶解氧的量,单位为mgO2/L。现有巢湖沿岸某电镀厂,不遵守环境法规,每周向湖中排放一次含氰废水,使近岸湖水含CN-的浓度为7.5×10-5mol/L,CN-与O2作用生成CO2、N2等。试问此电镀厂每排放一次废水将使近岸湖水的BOD增大多少?
(4)水质污染程度的另一重要指标为COD(化学耗氧量),它是指水中还原性物质(有机的和无机的),在规定条件下被氧化时,1L水样所消耗的氧的毫克数。测定COD通常有KMnO4法、K2Cr2C7法等。酸性KMnO4法:KMnO4在酸性溶液中经沸水浴加热,将发生:
2KMnO4+3H2SO4==K2SO4+2MnSO4+3H2O+5[O]。
①若为0.01000mol/L KMnO4溶液,则1.00mL相当于mgO2;
②若巢湖水样100mL,加入1:2 H2SO410mL,AgSO41g,混匀后,又加10mL 0.01000mol/L KMnO4溶液,在沸水中加热30min,取出加入10mL 0.02500mol/L Na2C2O4溶液,立即用0.01000mol/L KMnO4滴至微红色在15秒内不变色为终点,耗KMnO4液7.00mL,求巢湖水样的COD为多少?
已知2SO2(g)+O2(g)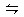 2SO3(g);△H<0的实验数据如下表:
2SO3(g);△H<0的实验数据如下表:
| 温度 |
不同压强下SO2的转化率(%) |
||||
| 1×105Pa |
5×105Pa |
1×106Pa |
5×106Pa |
1×107Pa |
|
| 450℃ |
97.5 |
98.9 |
99.2 |
99.6 |
99.7 |
| 550℃ |
85.6 |
92.9 |
94.9 |
97.7 |
98.3 |
(1)应选的温度是。
(2)应采用的压强是,理由是。
(3)在合成的SO3过程中,不需要分离出SO3的原因是。
在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K与温度t的关系如下:
CO(g)+H2O(g),其化学平衡常数K与温度t的关系如下:
| T/℃ |
700 |
800 |
830 |
1000 |
1200 |
| K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
请回答下列问题:
(1)该反应的化学平衡常数表达式K=。
(2)该反应为反应。(填“吸热”或“放热”)
(3)800℃时,固定容积的密闭容器中放入混合物,起始浓度为c(CO)=0.01 mol·L-1,c(H2O)=0.03 mol·L-1,c(CO2)=0.01 mol·L-1,c(H2)=0.05 mol·L-1,则反应开始时,H2O的消耗速率比生成速率(填“大”、“小”或“不能确定”)
(4)830℃时,在1L的固定容积的密闭容器中放入2mol CO2和1mol H2,平衡后CO2的转化率为,H2的转化率为。
将除去氧化膜的镁条投入到盛有稀盐酸的试管中,产生H2的速率变化情况如下图所示。
图中t1~t2速率变化的主要原因是___________,t2~t3速率变化的主要原因是_。