反应CO+H2O (g) 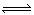 CO2+H2在800℃达到平衡时分别改变下列条件,K值发生变化的是
CO2+H2在800℃达到平衡时分别改变下列条件,K值发生变化的是
| A.将压强减小至原来的一半 | B.将反应温度升高至100℃ |
| C.添加催化剂 | D.增大水蒸气的浓度 |
下列现象与氢键有关的是:()
①NH3的熔、沸点比VA族其他元素氢化物的高
②小分子的醇、羧酸可以和水以任意比互溶
③冰的密度比液态水的密度小
④乙醇的沸点比甲醚的沸点高
⑤邻羟基苯甲醛的熔、沸点比对羟基苯甲醛的低
⑥水分子高温下也很稳定
| A.①②③④⑤⑥ | B.①②③④⑤ | C.①②③④ | D.①②③ |
碘单质在水溶液中溶解度很小,但在CCl4中溶解度很大,这是因为()
| A.CCl4与I2分子量相差较小,而H2O与I2分子量相差较大 |
| B.CCl4与I2都是直线型分子,而H2O不是直线型分子 |
| C.CCl4和I2都不含氢元素,而H2O中含有氢元素 |
| D.CCl4和I2都是非极性分子,而H2O是极性分子 |
膦(PH3)又称磷化氢,在常温下是一种无色有大蒜臭味的有毒气体,易燃烧
电石气的杂质中常含有磷化氢。它的分子构型是三角锥形。以下关于PH3的
叙述正确的是 ()
| A.PH3分子中有未成键的孤对电子 | B.PH3是非极性分子 |
| C.PH3是一种强氧化剂 | D.PH3分子的P-H键是非极性键 |
下列说法正确的是()
| A.ⅠA族元素的金属性比ⅡA族元素的金属性强 |
| B.ⅥA族元素的氢化物中,稳定性最好的其沸点也最高 |
| C.同周期非金属氧化物对应的水化物的酸性从左到右依次增强 |
| D.第三周期元素的离子半径从左到右逐渐减小 |
下列四种元素中,其单质的氧化性最强的是()
| A.基态原子含有未成对电子最多的第二周期元素 |
| B.位于元素周期表中第三周期第ⅢA族的元素 |
| C.基态原子最外层电子排布为2s22p6的元素 |
| D.基态原子最外层电子排布为3s23p5的元素 |