现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
请根据以上信息回答下列问题:
(1)写出下列物质的化学式: A 、 B 、C
(2)写出下列 反应离子方程式:
反应离子方程式:
反应③ ;反应⑤ 。
(3)检验F溶液中阳离子的方法: [来源:
(1)肼(N2H4)又称联氨,在常温下是一种液态燃料,可用作火箭燃料。已知在25℃时,101kPa时,1gN2H4在氧气中完全燃烧生成氮气和H2O,放出19.5kJ热量,表示N2H4燃烧热的热化学方程式是。
(2)肼-空气燃料电池是一种碱性燃料电池,肼-空气燃料电池放电时:正极的电极反应式:;负极的电极反应式:。
(3)下图是一个电解过程示意图。假设使用肼-空气燃料电池作为该过程中的电源,铜片质量变化为16g,则肼-空气燃料电池理论上消耗标准状况下的空气L。(假设空气中氧气体积分数为20%)
以乙炔为原料通过以下流程能合成有机物中间体D.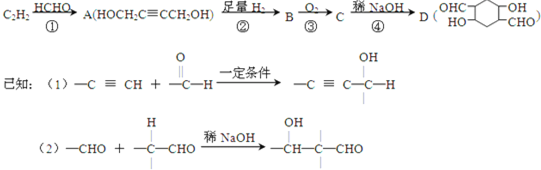
请回答下列问题:
(1)化合物D的分子式为,写出D中一种官能团的名称.
(2)写出生成A的化学反应方程式:.
(3)化合物B在浓硫酸催化下,加热与HOOCCOOH反应生成环状酯的化学方程式为(注明条件):
.
(4)化合物C的结构简式为:.
(5)已知1mol HCHO和1mol CH3CH2CHO发生类似已知(2)的反应,生成1molE.以下关于E的说法正确的是.
a、E能与H2发生加成反应,也能使酸性高锰酸钾溶液褪色.
b、E属于酯类物质.
c、1molE完全燃烧消耗5molO2.
d、生成E的反应属于取代反应.
有下列化学仪器:①托盘天平,②玻璃棒,③药匙,④烧杯,⑤量筒,⑥容量瓶,
⑦胶头滴管,⑧细口试剂瓶,⑨标签纸.
(1)现要配制500mL 1mol/L硫酸溶液,需用质量分数为98%、密度为1.84g/cm3的浓硫酸mL.
(2)从上述仪器中,按实验使用仪器的先后顺序.其编号排列是.
(3)若实验遇到下列情况,所配硫酸溶液的物质的量浓度偏小的有(填序号).
①用以稀释硫酸的烧杯未洗涤;
②未经冷却趁热将溶液注入容量瓶中;
③摇匀后发现液面低于刻度线再加水;
④容量瓶中原有少量蒸馏水;
⑤定容时仰视观察液面.
我国政府为了消除碘缺乏病,规定在食盐中必须加入适量的碘酸钾.检验食盐中是否加碘,可利用如下反应:KIO3+KI+H2SO4═K2SO4+I2+H2O.
(1)将上述氧化还原反应的化学方程式配平.
(2)该反应中,氧化剂和还原剂的物质的量之比为.
(3)如果反应中转移0.2mol电子,则生成I2的物质的量为.
(4)利用上述反应检验食盐中是否加碘,所需试剂是(填序号).
①碘水 ②KI溶液 ③淀粉溶液 ④稀硫酸 ⑤AgNO3溶液.
多晶硅(硅单质的一种)被称为“微电子大厦的基石”,制备中副产物以SiCl4为主,它环境污染很大,能遇水强烈水解,放出大量的热。研究人员利用SiCl4水解生成的盐酸和钡矿粉(主要成分为BaCO3,且含有铁、镁等离子),制备BaCl2 • 2H2O,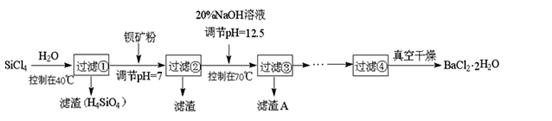
工艺流程如下:
已知:①常温下Fe3+、Mg2+ 完全沉淀的pH分别是3.4、12.4;
②BaCO3的相对分子质量是197; BaCl2 • 2H2O的相对分子质量是244;
(1)SiCl4发生水解反应的化学方程式。
(2)氮化硅(Si3N4)是一种高温结构材料,粉末状的Si3N4可以在高温条件下由SiCl4 蒸
汽与NH3反应得到,请写出该反应的化学方程式。
(3)加钡矿粉调节pH=7的作用是:
①使BaCO3转化为BaCl2
②_______________________________
(4)生成滤渣A的离子方程式________________________________________
(5)BaCl2滤液经____________________、______________________、过滤、洗涤,再经真空干燥后得到BaCl2 • 2H2O
(6)10吨含78.8% BaCO3的钡矿粉理论上最多能生成BaCl2 • 2H2O___________吨。