A、B、C、D、E五种元素,它们原子的核电荷数依次递增且均小于18。A元素原子核外只有1个电子;C是地壳中含量最多的元素;B、C可形成两种化合物BC和BC2,B的最高正价与最低负价绝对值相等,BC有毒,BC2可用于灭火;D元素的最外层电子数是其电子层数的三分之一;E—具有与Ar原子相同的电子层结构。
(1)写出A、C两种元素的符号:A , C 。
(2)写出D原子和E—离子的结构示意图:D原子 ,E—离子 。
(3)由A、B、C、D四种元素组成的常见化合物的化学式为 ,
其电离方程式为 。
(4)写出A、C、D三种元素组成的常见化合物的稀溶液,常温下和E的单质反应的化学方程式 。
和
元素在化学中占有极其重要的地位。 (1)写出
的基态原子核外电子排布式。
(1)写出
的基态原子核外电子排布式。 从电负性角度分析,
、
和
元素的非金属活泼性由强至弱的顺序为。
从电负性角度分析,
、
和
元素的非金属活泼性由强至弱的顺序为。 (2)
的晶体结构与晶体硅的相似,其中
原子的杂化方式为,微粒间存在的作用力是。
(2)
的晶体结构与晶体硅的相似,其中
原子的杂化方式为,微粒间存在的作用力是。 (3)氧化物
的电子总数与
的相等,则
为填元素符号)。
是优良的耐高温材料,其晶体结构与
晶体相似。
的熔点比
的高,其原因是。
(3)氧化物
的电子总数与
的相等,则
为填元素符号)。
是优良的耐高温材料,其晶体结构与
晶体相似。
的熔点比
的高,其原因是。 (4)
、
为同一主族的元素,
和
化学式相似,但结构和性质有很大不同。
中
与
原子间形成
(4)
、
为同一主族的元素,
和
化学式相似,但结构和性质有很大不同。
中
与
原子间形成 键和
键,
中
与
原子间不形成上述
健。从原子半径大小的角度分析,为何
、
原子间能形成,而
、
原子间不能形成上述
键。
键和
键,
中
与
原子间不形成上述
健。从原子半径大小的角度分析,为何
、
原子间能形成,而
、
原子间不能形成上述
键。

 金属铝的生产是以
为原料,在熔融状态下进行电解:
金属铝的生产是以
为原料,在熔融状态下进行电解:
请回答下列问题: (1)冰品石(
)的作用是。
(1)冰品石(
)的作用是。 (2)电解生成的金属铝是在熔融液的(填"上层"或"下层")。
(2)电解生成的金属铝是在熔融液的(填"上层"或"下层")。 (3)阴极和阳极均由材料做成;电解时所消耗的电极是(填"阳极"或"阴极")。
(3)阴极和阳极均由材料做成;电解时所消耗的电极是(填"阳极"或"阴极")。 (4)铝是高耗能产品,废旧铝材的回收利用十分重要。在工业上,最能体现节能减排思想的是将回收铝做成(填代号)。
(4)铝是高耗能产品,废旧铝材的回收利用十分重要。在工业上,最能体现节能减排思想的是将回收铝做成(填代号)。 a.冰品石 b.氧化铝 c.铝锭 d.硫酸铝
a.冰品石 b.氧化铝 c.铝锭 d.硫酸铝
干电池应用广泛,其电解质溶液是
混合溶液。 (1)该电池的负极材料是。电池工作时,电子流向(填"正极"或"负极")。
(1)该电池的负极材料是。电池工作时,电子流向(填"正极"或"负极")。 (2)若
混合溶液中含有杂质
,会加速某电极的腐蚀,其主要原因是。欲除去
,最好选用下列试剂中的(填代号)。
(2)若
混合溶液中含有杂质
,会加速某电极的腐蚀,其主要原因是。欲除去
,最好选用下列试剂中的(填代号)。 .
.
.
.
.
.
.
.
(3)
的生产方法之一是以石墨为电极,电解酸化的
溶液。阴极的电极反应式是 。若电解电路中通过2
电子,
的理论产量为。
。若电解电路中通过2
电子,
的理论产量为。
运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义。 (1)合成氨反应反应
(1)合成氨反应反应
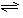 ,若在恒温、恒压条件下向平衡体系中通入氩气,平衡移动(填"向左""向右"或"不");,使用催化剂反应的
(填"增大""减小"或"不改变")。
,若在恒温、恒压条件下向平衡体系中通入氩气,平衡移动(填"向左""向右"或"不");,使用催化剂反应的
(填"增大""减小"或"不改变")。 (2)
(2)
 则反应
的
=
。
则反应
的
=
。 (3)在25℃下,向浓度均为0.1
的
和
混合溶液中逐滴加入氨水,先生成沉淀(填化学式),生成该沉淀的离子方程式为。已知25℃时
=1.8×10-11,
=2.2×10-20。
(3)在25℃下,向浓度均为0.1
的
和
混合溶液中逐滴加入氨水,先生成沉淀(填化学式),生成该沉淀的离子方程式为。已知25℃时
=1.8×10-11,
=2.2×10-20。
 (4)在25℃下,将
的氨水与0.01
的盐酸等体积混合,反应平衡时溶液
则溶液显性(填"酸""碱"或"中");用含
的代数式表示
的电离常数
=。
(4)在25℃下,将
的氨水与0.01
的盐酸等体积混合,反应平衡时溶液
则溶液显性(填"酸""碱"或"中");用含
的代数式表示
的电离常数
=。
四川汶川盛产品质优良的甜樱桃。甜樱桃中含有一种羟基酸(用
表示),
的碳链结构无支链,化学式为
;1.34 g
与足量的碳酸氢钠溶液反应,生成标准状况下的气体0.448 L。
在一定条件下可发生如下转化:



 其中,
、
、
、
分别代表一种直链有机物,它们的碳原子数相等。
的化学式为
(转化过程中生成的其它产物略去)。
其中,
、
、
、
分别代表一种直链有机物,它们的碳原子数相等。
的化学式为
(转化过程中生成的其它产物略去)。 已知:
已知:

的合成方法如下:
①


②
其中,
、
、
分别代表一种有机物。 请回答下列问题:
请回答下列问题:
 (1)
的结构简式是。
(1)
的结构简式是。 (2)
生成
的化学方程式是。
(2)
生成
的化学方程式是。
 (3)
与乙醇之间发生分子间脱水,可能生成的有机物共有种。
(3)
与乙醇之间发生分子间脱水,可能生成的有机物共有种。 (4)
的结构简式是。
(4)
的结构简式是。
 (5)写出
与水反应生成
和
的化学方程式:。
(5)写出
与水反应生成
和
的化学方程式:。