某学习小组在探究CO2与NaOH溶液反应的实验中,先用铝制易拉罐收集满一罐CO2气体,然后迅速向其中加入—定量的NaOH浓溶液,立即将易拉罐口封闭(不漏气),轻轻摇动易拉罐,发现易拉罐很快变瘪,但过一段时间后,易拉罐又重新鼓起来(反应过程中温度的变化忽略不计)。
(提出问题)易拉罐为什么先瘪后鼓?
(分析猜想)易拉罐开始时变瘪的原因是 (用化学方程式表示),
易拉罐重新鼓起的原因是易拉罐中又生成了气体A,其成分极有可能是CO2或H2。
(查阅资料)①Na2CO3具有较强的热稳定性,只有在高温条件下才会分解;
②铝单质比较容易被酸、碱腐蚀。
(设计方案并进行实验)为了检验铝制易拉罐中重新生成的气体成分,小组又进行如下实验,并记录了相应的实验现象:
| 实验步骤 |
实验现象 |
实验结论 |
| 将易拉罐口打开,迅速用燃着的木条伸入罐口。 |
发出“噗”的—声,产生淡蓝色火焰,片刻后熄灭。 |
说明罐中重新生成的气体A是 (2) |
| 取少量铝片于试管中,先加入适量的水,片刻后再加入少量的氢氧化钠溶液。 |
先加水,没有明显变化,后加入氢氧化钠溶液后产生无色无味的气体。 |
说明铝是否与水直接反应:(3)(填“是”或“否”),铝能够与 ⑷ 溶液反应。 |
| 取少量易拉罐中反应后的溶液于试管中,加入过量的稀盐酸。 |
产生了无色无味气体,该气体能使澄清石灰水变浑浊。 |
说明原CO2气体被NaOH溶液吸收 |
[实验结论]①铝制易拉罐变瘪的原因是CO2被NaOH溶液吸收,②铝制易拉罐重新鼓起的原因是铝与NaOH溶液反应产生了气体。
[反思评价]小组根据实验探究获得一条对金属铝化学性质的新认识: (5) 。
[拓展延伸] A1与NaOH溶液反应产生了气体的同时还生成另一种书写形式类似于KMnO4的盐,请完成下列反应化学方程式:2Al+2NaOH+2H2O = 2 (6) +3A↑。当然,本实验只是初步探究,还有进一步探究的价值,有待我们在以后的学习中去深究。
在学习过程中,小明同学提出一个问题:“碳燃烧时可能生成CO2,也可能生成CO,那么碳与氧化铜反应生成的气体是否也有多种可能?”
[猜想]碳与氧化铜反应生成的气体中:①只有CO2;②既有CO,又有CO2;③只有CO。
[查阅资料]浸有磷钼酸溶液的氯化钯试纸遇CO2无变化,但遇到微量CO会立即变成蓝色。
[方案设计]通过上述资料和已有知识,小明初步设想用浸有磷钼酸溶液的氯化钯试纸和澄清石灰水对碳与氧化铜反应生成的气体进行检验。根据小明的设想,请你填空:
(1)若试纸不变色,澄清石灰水变浑浊,则只有CO2;
(2)若试纸变成蓝色,澄清石灰水变浑浊,则既有CO,又有CO2;
(3)若试纸_____________,澄清石灰水_____________,则只有CO。
[实验验证]经过思考之后,小明设计了下图实验装置:
实验步骤:(1)打开弹簧夹,先通一会儿纯净、干燥的N2;
(2)关闭弹簧夹,点燃酒精灯加热。
[结论]小明通过分析实验现象,确认猜想②是正确的,请你写出装置C中发生反应的化学方程式:___________________________________________;
[反思与评价](1)该实验开始前通一会儿N2的目的是:_______________________;
(2)请从环保的角度分析该实验装置中的不完善之处_____________________________。
某气体由H2、CO中的一种或两种组成,某学校化学兴趣小组对该气体的组成
进行探究。
【猜想】① 气体中只有H2;② 气体中只有CO;③ 气体中既有H2,又有CO.
【查阅资料】白色无水硫酸铜遇水会变蓝色。
【实验设计】通过上述资料和已有化学知识,设计了以下装置进行实验。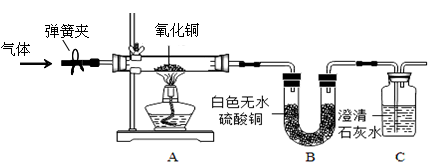
根据以上设计,请完成填空:
(1)若无水硫酸铜变蓝色,石灰水不变浑浊,则猜想①正确。
(2)若无水硫酸铜,石灰水 ,则猜想②正确。
(3)若无水硫酸铜,石灰水 ,则猜想③正确。
【实验步骤】
①打开弹簧夹,先通一会儿气体;②关闭弹簧夹,点燃酒精灯加热。
【实验结论】
通过对实验现象进行分析,确认猜想③正确。
实验过程中,玻璃管中的现象是;
请写出装置C中发生反应的化学方程式。
【反思与评价】
(1)该实验开始通一会儿气体的目的是。
(2)从环保的角度分析该实验装置的不完善之处是。
(3)该实验装置中,若将装置B、装置C对调,将(填“能”或“不能”)得到正确结论,原因是。
(8分)小聪同学家新换了水龙头,从说明书上了解到该水龙头是铜质镀铬。好奇的小聪想探究铬(Cr)与常见金属铁、铜的活动性强弱,邀请你一同参加。
【作出猜想】
猜想一:Cr>Fe>Cu;猜想二:Fe>Cu>Cr;猜想三:你的猜想是。
【查阅资料】
铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜。
铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液。
【设计与实验】
小聪同学取大小相等的三种金属片,用砂纸打磨光亮,分别放入等量的同种稀硫酸。
【结论与解释】
(1)小聪得到的结论是猜想正确。
(2)实验前用砂纸打磨金属片的目的是。
【知识运用】
将铬片投入FeSO4溶液中,反应(填“能”或“不能”)进行。若能进行,请你写出反应的化学方程式。
早在春秋战国时期,我国就开始生产和使用铁器。工业上炼铁的原理是利用一氧化碳和氧化铁的反应。某化学兴趣小组利用下图装置进行实验探究,请按要求填空: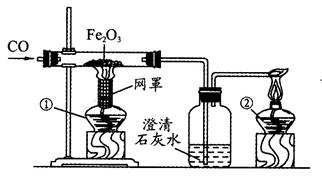
(1)写出CO还原Fe2O3的化学方程式;
(2)实验中盛澄清石灰水的试管中可观察到的现象是;
(3)右边导气管口放置点燃的酒精灯的目的是;实验时,应先点燃第个酒精灯。
(4)某同学用此图进行实验,开始时玻璃管中产生了黑色粉末,但过了一会儿,黑色粉末又变为了红色。出现这种现象的原因
某校研究性学习小组在做“寻找新的催化剂”课题时,发现将生锈的铁钉放到过氧化氢溶液中,也可以加快过氧化氢的分解速率.于是,他们对此展开探究:
【提出问题】生锈的铁钉中,哪种物质能做H2O2分解的催化剂?与二氧化锰相比哪种物质更适合H2O2做分解的催化剂?
【提出猜想】猜想一:林菲同学:铁钉表面的Fe2O3是H202溶液分解反应的催化剂。
猜想二:小华同学:铁钉中的铁是H202分解的催化剂。
| 实验编号 |
操作步骤 |
实验现象 |
| 实验1 |
将带火星的木条伸入盛有10mL 5%的H2O2溶液的试管内,观察现象 |
木条不复燃 |
| 实验2 |
在盛有1克Fe2O3固体的试管中加入10mL5%的H2O2溶液,再将带火星的木条伸入试管内,观察现象. |
有大量气泡产生,带火星的木条复燃 |
| 实验3 |
在盛有1克_____的试管中加入10mL 5%的H2O2溶液,再将带火星的木条伸入试管内,观察现象. |
木条不复燃 |
【分析与结论】
(1)设计“实验1”的目的是_____。
(2)由上述实验可知,猜想____错误。实验(2)反应的化学方程式为_____
(3)同学们讨论后认为,林菲同学的“实验2”还不能够确切的证明氧化铁就是过氧化氢分解制取氧
气的催化剂,理由是:_____。
(4)小华通过仔细观察发现“实验3”中一直没有变化的试管,过了一段时间后试管中也出现了气体,小华觉得很奇怪,你能猜想其中的原因吗?( 如果你能正确回答下列问题,你将得到4分奖励,但本卷总分不超过60分)
(5)请设计实验探究Fe2O3和MnO2,哪种物质更适合做H2O2分解的催化剂?__________