I、磷、硫元素的单质和化合物应用广泛。
(1)磷酸钙与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,反应为:
2Ca3(PO4)2+6SiO2 6CaSiO3+P4O10 10C+P4O10
6CaSiO3+P4O10 10C+P4O10 P4+10CO
P4+10CO
每生成1mol P4时,就有__________mol电子发生转移。
(2)硫代硫酸钠(Na2S2O3)是常用的还原剂。在维生素C(化学式C6H8O6)的水溶液中加入过量I2溶液,使维生素C完全氧化,剩余的I2用Na2S2O3溶液滴定,可测定溶液中维生素C的含量。发生的反应为:C6H8O6+I2 C6H6O6+2H++2I- 2
C6H6O6+2H++2I- 2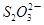 +I2
+I2
 +2I-在一定体积的某维生素C溶液中加入a mol·L-1 I2溶液V1mL,充分反应后,用Na2S2O3溶液滴定剩余的I2, 消耗b mol·L-1Na2S2O3溶液V2mL。该溶液中维生素C的物质的量是___________mol。
+2I-在一定体积的某维生素C溶液中加入a mol·L-1 I2溶液V1mL,充分反应后,用Na2S2O3溶液滴定剩余的I2, 消耗b mol·L-1Na2S2O3溶液V2mL。该溶液中维生素C的物质的量是___________mol。
(3)在酸性溶液中,碘酸钾(KIO3)和亚硫酸钠可发生如下反应:2 +5
+5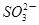 +2H+
+2H+ I2+5
I2+5 +H2O生成的碘可以用淀粉溶液检验,根据反应溶液出现蓝色所需的时间来衡量该反应的速率。某同学设计实验如下表所示:
+H2O生成的碘可以用淀粉溶液检验,根据反应溶液出现蓝色所需的时间来衡量该反应的速率。某同学设计实验如下表所示: 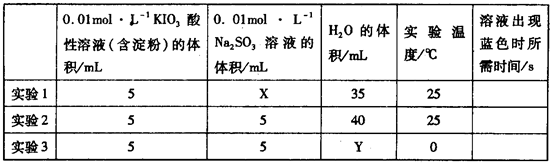
该实验的目的是______________;表中X=__________mL
Ⅱ、稀土元素是宝贵的战略资源,我国的蕴藏量居世界首位。
(4)铈(Ce)是地壳中含量最高的稀土元素。在加热条件下CeCl3易发生水解,无水CeCl3可用加热CeCl3·6H2O和NH4Cl固体混合物的方法来制备。其中NH4Cl的作用是_______________________.
(5)在某强酸性混合稀土溶液中加入H2O2,调节pH≈3,Ce3+通过下列反应形成Ce(OH)4沉淀得以分离。完成反应的离子方程式: Ce3++
Ce3++ H2O2+
H2O2+ H2O
H2O
 Ce(OH)4↓+
Ce(OH)4↓+ ______________
______________
A、B、C、D、E都是元素周期表中前20号元素,原子序数依次增大,A是地壳中含量最高的元素,B、C、D同周期,E和其他元素既不在同一周期也不在同一主族,D的氢化物及其最高价氧化物对应的水化物均为强酸,且B、C、D的最高价氧化物对应的水化物两两混合均能发生反应生成盐和水。据此回答下列问题:
(1)A和D的氢化物中,沸点较低的是(选“A”或“D”)。
(2)元素C在元素周期表中的位置是,B的最高价氧化物对应的水化物的电子式为。
(3)A、D、E可以形成多种盐,其中一种盐中A、D、E三种元素的原子个数比为2:2:1,该盐的名称为。它的水溶液与D的氢化物的水溶液反应可生成D的单质,该反应的离子方程式为。
X、Y、Z、W是四种短周期元素,X原子M层上的电子数是原子核外电子层数的2倍;Y原子最外层电子数是次外层电子数的2倍;Z元素的单质为双原子分子,Z的氢化物水溶液呈碱性;W元素最高正价是+7价。回答下列问题:
(1)元素X原子结构示意图为__________。
(2)元素Y的一种同位素可测定文物年代,这种同位素的符号是________。
(3)元素Z能与氢元素形成+1价阳离子,每个该离子中的电子数是________,元素Z的最高价含氧酸的稀溶液与金属银反应的离子方程式为_______________________________。
(4)元素W的单质与元素X的低价氧化物在水溶液中反应的离子方程式_____________________;元素X的气态氢化物与过氧化氢溶液混合后有浅黄色固体生成,请写出发生的化学方程式_________。
(5)探寻物质的性质差异性是学习的重要方法之一。X、Y、Z、W四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种酸的是________(用酸的分子式表示)。
(1)在水溶液中,YO3n—和S2-发生反应的离子方程式如下:
YO3n—+3S2-+6H+=Y-+3S↓+3H2O,已知Y为1~18号元素。
(a)YO3n—中Y的化合价是__________; Y元素原子的最外层电子数是____________;
(b)S2-的半径__________Y-的半径(填“大于”或“小于”)。
(2)在一定条件下A与B反应可生成C和D,其能量变化如下图
(a)若E1>E2,反应体系的总能量____(填“升高”“降低”),为___(填“吸热”“放热”)反应。
(b)若E1<E2,反应体系的总能量___(填“升高”“降低”),为______(填“吸热”“放热”)反应。
已知X、Y、Z、W四种元素分布在元素周期表中的三个不同短周期元素里,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子最外层电子数之和。Y的氢化物分子中有3个共价键。Z原子最外层电子数是次外层电子数的3倍。试推断:
(1)X、Y两种元素的名称:X、Y;
(2)W在元素周期表中的位置是;
(3)由X、Y、Z所形成的属于强电解质的共价化合物的化学式是,它与W的最高氧化物的水化物的溶液反应时的离子方程式:。
下表是元素周期表的一部分(注意:用元素符号或化学式填空)
 族 族周期 |
ⅠA |
ⅡA |
ⅢA |
IVA |
VA |
VIA |
VIIA |
O族 |
| 1 |
||||||||
| 2 |
G |
H |
D |
|||||
| 3 |
B |
C |
E |
|||||
| 4 |
F |
A |
||||||
(1)C的离子的结构示意图,G元素的氧化物化学式,H的氢化物的化学式。
(2)H元素的单质的电子式;
(3)A-H八种元素中(a)原子半径最大的元素是,(b)单质的还原性最强的元素是,(c)最高价氧化物对应水化物酸性最强的是;(d)最高价氧化物对应水化物碱性最强的是。
(4)用电子式表示AE 2的形成过程。
(5)B与C的最高价氧化物对应水化物反应的离子方程式。