有一混合溶液是由硝酸、碳酸钠、硫酸、氯化铜四种物质中的两种混合而成,向该混合溶液中滴入Ba(OH)2溶液,产生沉淀的质量与加入 Ba(OH)2溶液体积的关系如图所示,据此回答:
(1)该混合溶液是由________和____ ___组成的。
(2)不含另外两种物质的理由:
一是________________________
二是_________________________________
请结合下图回答问题: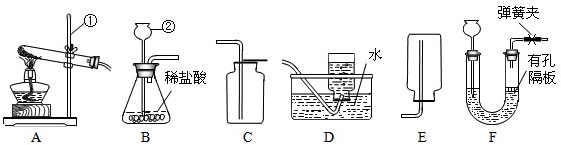
(1)标号①②的仪器名称:①,②.
(2)实验室选用
装置制取
,气体收集完毕时,应先(填"从水中取出导气管"或"熄灭酒精灯").
(3)实验室可用
固体和熟石灰混合加热制取
,应选择发生装置为(选填序号).
(4)选择发生装置
和收集装置(选填序号)可以用于实验室制取
,若将发生装置由
改为
,其优点是.
①为了得到纯净、干燥的
,除杂装置(如图)的导管按气流方向连接顺序是(选填字母);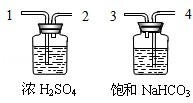
a.1→2→4→3 b.2→1→3→4
c.4→3→1→2 d.3→4→2→1
用化学反应方程式表示饱和
溶液的作用.
②写出用澄清石灰水检验
的化学反应方程式.
向
粉与过量稀
反应后的溶液中滴加
溶液,溶液由浅绿色变为黄色,无气泡产生;继续滴加
溶液,有气泡出现;反应后滴加
溶液有白色沉淀.
(1)溶液由浅绿色变为黄色的化学反应方程式:.
(2)产生气泡的化学反应方程式:.
科学家设想利用太阳能加热器"捕捉
"、"释放
",实现碳循环.
(1)步骤1的化学方程式为.
(2)为确定步骤2中的碳酸钙是否完全分解,设计的实验步骤为:取少量固体于试管中,滴加过量溶液,若观察到试管内.则分解不完全.
(3)上述设想的优点有(填字母序号).
| A. |
原料易得且可循环利用 |
B. |
充分利用太阳能 |
C. |
可全地域全天候使用 |
(4)
是宝贵的碳氧资源.
和
在一定条件下可合成甲酸(
),此反应中
与
的分子个数比为,若要检验1%甲酸水溶液是否显酸性,能选用的有(填字母序号).
| A. |
无色酚酞溶液 |
B. |
紫色石蕊溶液 |
C. |
试纸 |
(5)请列举
的另两种用途,.
请根据下列实验装置图回答问题.
(1)写出仪器a、b的名称:a,b.
(2)用A装置制取O2的化学方程式为,应选用的收集装置为(填装置编号).用B装置制取CO2的化学方程式为.
(3)如图F是"铁丝在氧气中燃烧"实验的改进装置.实验时,打开分夜漏斗活塞,通入干燥氧气约10秒,引燃铁丝下端火柴杆,伸入塑料瓶内,并对准玻璃管口正上方,观察到的现象是:
铁丝剧烈燃烧,.
改进后的优点是(填序号).
①氧气无需提前制备和收集,操作更方便
②塑料瓶代替集气瓶,防止集气瓶炸裂,更安全
③装置集氧气的制取、干燥和性质验证于一体,实验更优化
(4)某兴趣小组同学将带火星的木条伸入到收集满氧气的集气瓶内,木条复燃,拿出木条,盖好集气瓶.过一会儿,再用带火星的木条伸入瓶内,木条仍然复燃.重复以上操作,直到木条不再复燃.据此现象 你能得到的结论是.
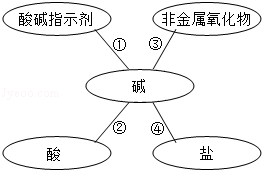
某化学兴趣小组学习酸、碱、盐性质后,通过实验对碱的化学性质进行验证和总结,如图所示(已知:
溶液呈中性,
).
(1)甲同学将酚酞试液滴入
溶液中,观察到溶液变红,得出结论:
溶液呈(填"酸性"、"碱性"或"中性");
(2)乙同学将过量的稀盐酸加入到甲同学所得溶液中,观察到红色褪去,此时所得溶液中含有的溶质有(酸碱指示剂除外);
(3)丙同学根据反应③得出结论:实验室存放碱溶液时需;
(4)丁同学将
溶液加入
溶液中,充分反应后,与乙同学所得溶液混合,静置后发现:上层为无色透明的溶液,底部有白色沉淀.则上层溶液中一定含有的溶质是(酸碱指示剂除外),可能含有的溶质是;为验证可能含有的溶质,应该补充的实验操作是.