A、B、C、D、E是Na的单质及其化合物,它们有如图所示的相互转化关系。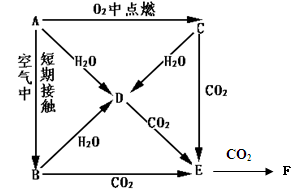
(1) 写出以下物质的化学式:C F
(2) 完成以下离子方程式:
C→D:
D→E:
(3) 等质量的A和B分别投入到等质量且足量的水中,反应后所得溶液溶质质量分数分别为
ω1、ω2,则ω1 ω2 (填“>”或“<”或“==”)。
(4) E中混有少量的F,用化学方程式表示除去F的两种方法:
、
(5) 用m g的D来制取纯净的E,写出最简单的实验方法
我国规定饮用水质量标准必须符合下列要求:
| pH |
6.5~6.8 |
| Ca2+、Mg2+总浓度 |
<0.0045mol/L |
| 细菌总数 |
<100个/L |
以下是源水处理成自来水的工艺流程示意图:
源水→曝气池 一级沉降池
一级沉降池 二级沉降池
二级沉降池 过滤池→自来水
过滤池→自来水
(1)源水中含Ca2+ 、Mg2+、HCO3-、Cl-等,加入石灰后生成Ca(OH)2,进而发生若干复分解反应,写出其中一个离子方程式。
(2)凝聚剂除去悬浮固体颗粒的过程(填写编号,多选倒扣分)
①只是物理过程 ②只是化学过程 ③是物理和化学过程
FeSO4.7H2O是常用的凝聚剂,它在水中最终生成沉淀。
(3)通入二氧化碳的目的是和。
(4)气体A的作用是。这种作用是基于气体A和水反应的产物
具有性.
(5)下列物质中,可以作为气体A的代用品。(填写编号,多选倒扣分)
①Ca(ClO)2 ②NH3 (液) ③K2FeO4 ④SO2
(1)某学生用托盘天平称量一个小烧杯的质量,如小烧杯的质量为32.6g,用“↓”表示在托盘上放砝码,“↑”表示从托盘上取砝码,请用箭头在下表中填空,表示称量过程,并在图3—2所示的游码尺上画出游码的位置(画“|”表示)。
| 砝码质量/g |
50 |
20 |
20 |
10 |
5 |
| 取用砝码情况 |

(2)图3—3表示10mL量筒中液面的位置,A与B,B与C刻度间相差1mL,如果刻度A为4,量筒中的液体的体积是__________mL。
(3)用18mol•L—1的硫酸溶液配制0.5mol•L—1的硫酸溶液250mL所需的玻璃仪器为___________。
(1)实验室制取氢氧化铁胶体的化学方程是,
可用(方法)证明胶体已经制成。
有人在研究硫酸亚铁受热分解反应时,作了两种假设:
(2)假设它按氯酸钾受热分解的方式来分解,反应的化学方程式为:
(3)假设它按碳酸钙受热分解的方式来分解,反应的化学方程式为:
(4)事实上,硫酸亚铁分解为氧化铁,二氧化硫,三氧化硫(分解温度为500℃左右),则反应化学方程式为:
(1)氯气可溶于水,常温下,1体积水中溶解2体积的氯气,溶于水的氯气一部分与水反应,该化学方程式是。
(2)多余氯气常用NaOH溶液吸收,写出化学方程式
(3)氯水中含有多种成分。将紫色石蕊试液滴入氯水中,溶液显红色起作用的成分是____________;过一会儿,溶液颜色逐渐褪去,起作用的成分是____________;往氯水中滴入硝酸银溶液,产生白色沉淀,起作用的成分是________________。
有关物质的量的计算。
(1)有NaCl、CaCl2、AlCl3三种溶液,若溶质的物质的量相等,分别与足量的硝酸银溶液反应,则生成沉淀的物质的量之比为________________.若生成的沉淀的质量相等,则三种溶液中溶质的物质的量之比为__________。
(2)相同质量的SO2和SO3,所含分子的数目之比为_________;所含O的物质的量之比为________。
(3)下列各物质所含原子数目,按由大到小顺序排列的是
①0.5mol NH3②标准状况下22.4L He③4℃9mL水④0.2mol H3PO4