提纯下列物质(括号内为杂质),填写所选用的除杂试剂和除杂方法
| |
括号内为杂质 |
除杂试剂 |
操作 |
| 1 |
甲烷(乙烯) |
|
|
| 2 |
粗苯甲酸 |
—— |
|
| 3 |
苯(甲苯) |
|
|
| 4 |
乙醇(水) |
|
|
下列是元素周期表的二、三、四周期中的部分元素
(1)表中所标出的元素当中,最活泼的金属元素是________,最活泼的非金属元素是________,最不活泼的元素是________;
(2)C与N相比,原子半径 较小的是;
较小的是;
(3)K和Mg两种元素的最高价氧化物对应的水化物都是碱,则这两种碱的碱性强弱为:KOHMg(OH)2 (大于/小 于);
于);
(4)已知①2H2+O2 2H2O;②Cl2和H2混合,在光照下就可以发生爆炸,生成HCl。据此推断,活泼性比较:O2Cl2 (大于/小于);
2H2O;②Cl2和H2混合,在光照下就可以发生爆炸,生成HCl。据此推断,活泼性比较:O2Cl2 (大于/小于);
另由③Cl2+2NaBr=Br2+2NaCl,可推断氧化性比较:Cl2 Br2 (大于/小于)。
现有下列两组物质:①H2、CaCO3、HCl、NH3②氯化钠溶液、硫酸铜溶液、氢氧化铁胶体、硫酸铁溶液。请你从组成的元素、物质的性质等多个角度用两种不同的分类标准从每组中选出一种不同类的物质,并指出其分类依据,写在下面相应的表格内。
| 组别 |
被选出的物质 |
分类依据 |
| 第①组 |
||
| 第②组Com] |
||
(1)(8分) 某无色透明溶液可能存在Na+、Fe3+、Ba2+、NO3-、CO32-、HCO3-、SO42-中的几种离子,现有如下操作:
Ⅰ、取适量该溶液加入CaCl2溶液无沉淀,继续滴加盐酸产生无色无味的气体。
Ⅱ、另取该溶液滴加一定量的NaOH溶液有白色沉淀生成。
试回答下列问题:
①该溶液中一定存在的离子有__________,一定不存在的离子__________。
②用一个离子方程式表示操作②的实验现象:
______________________________________________________。
(2)下列各项中的两种物质在溶液中的反应,可用同一离子方程式表示的是(),请写出该离子反应方程式:___________________________ __________________。
__________________。
| A.盐酸和烧碱溶液、硫酸和氢氧化钡溶液 |
B.纯 碱溶液和盐酸、石灰石和硫酸 碱溶液和盐酸、石灰石和硫酸 |
| C.氯化钡溶液和硫酸钠溶液、硝酸钡溶液和硫酸 |
| D.碳酸铵溶液和氢氧化钠溶液、碳酸铵溶液和氢氧化钙溶液 |
天然气化工是重要的支柱产业之一,以天然气为原料经下列反应路线可得工程塑料PBT。 (1)B分子结构中只有一种氢、一种氧、一种碳,则B的结构简式是;B的同分异构体中与葡萄糖具有类似结构的是(写结构简式)。
(1)B分子结构中只有一种氢、一种氧、一种碳,则B的结构简式是;B的同分异构体中与葡萄糖具有类似结构的是(写结构简式)。
(2) F的结构简式是;PBT属于类有机高分子化合物.
F的结构简式是;PBT属于类有机高分子化合物.
(3)由A、D生成E的反应方程式为,其反应类型为 。
。
(4)E的同分异构体G不能发生银镜反应,能使溴水褪色,能水解且产物的碳原子数不等,则G在NaOH溶液中发生水解反应的化学方程式是
图表法、图象法是常用的科学研究方法。
下表列出前20号元素中的某些元素性质的一些数据:
| 元素 性质 |
A |
B[ |
C |
D |
E |
F |
G |
H |
I |
J |
| 原子半径(10-10m) |
1.02 |
2.27 |
0.74 |
1.43 |
0.77 |
1.10 |
0.99 |
1.86 |
0.75 |
1.17 |
| 最高价态 |
+6 |
+1 |
— |
+3 |
+4 |
+5 |
+7 |
+1 |
+5 |
+4 |
| 最低价态 |
-2 |
— |
-2 |
— |
-4 |
-3 |
-1 |
— |
-3 |
-4 |
试回答下列问题:
(1)已知H为Na元素,则以上10种元素中第一电离能最小的是:(填编号)。比元素B原子序数大10的元素其基态原子的核外电子排布是 。
。
(2)由上述C、E、G三种元素中的某两种元素形成的化合物中,每个原子的最外层都满足8电子稳定结构的可能是(写分子式,写出一种即可),元素G、I分别和J形成的两种化合物的晶体类型分别是。
(3)元素E与C及氢元素可形成一种相对分子质量为60的一元羧酸分子。其一分子中共形
成 个σ键,个π键。
个σ键,个π键。
(4)短周期某主族元素K的电离能情况如图(A)所示。
则K元素位于周期表的第族。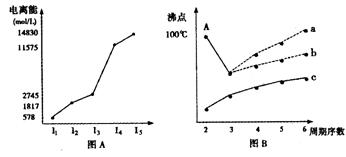
图B是研究部分元素的氢化物的沸点变化规律的图像,折线c可以表达出第族元素氢化物的沸点的变化规律。
不同同学对某主族元素的氢化物的沸点的变化趋势画出了两条折线—折线a和折线b,你认为正确的是,理由是